Genome-wide identification and expression analysis of the MAP70 gene family in Brassica napus L.
-
摘要:
采用生物信息学方法,从甘蓝型油菜(Brassica napus L.)基因组数据库中筛选鉴定MAP70s基因家族成员,对鉴定得到的BnaMAP70s基因家族成员的序列特征进行生物信息学分析,同时利用qRT-PCR方法分析该基因家族成员在不耐渍和强耐渍甘蓝型油菜品种幼苗中的基因表达水平。结果显示,本研究共鉴定得到19个BnaMAP70基因家族成员,分布在11条染色体上,可分为5个亚家族。BnaMAP70s启动子的上游存在厌氧胁迫、响应植物激素等相关元件,表明BnaMAP70s可能参与植株生长发育和渍水胁迫调控;转录水平存在品种特异性、植株部位特异性、时间特异性。qRT-PCR分析结果表明,BnaMAP70-1和BnaMAP70-4在渍水胁迫下出现表达差异,说明这两个基因受渍水胁迫的调控。
-
关键词:
- 甘蓝型油菜 /
- BnaMAP70s基因家族 /
- 耐渍 /
- 生物信息学
Abstract:MAP70 family members were screened and identified using bioinformatics based on the genomic database of Brassica napus L., with bioinformatics analysis performed on the sequence characteristics of the identified BnaMAP70 gene family members. Expression levels of the BnaMAP70 genes were analyzed using qRT-PCR in seedling varieties with waterlogging sensitivity and tolerance. In total, 19 members of the BnaMAP70 gene family were identified, distributed on 11 chromosomes and divided into five subfamilies. The upstream elements involved in anaerobic stress and phytohormones of the BnaMAP70 promoter indicated that they may be involved in plant growth, development, and regulation of waterlogging stress. The transcription levels of genes were species-specific, plant site-specific, and time-specific. The qRT-PCR results showed that BnaMAP70-1 and BnaMAP70-4 were differentially expressed under waterlogging stress, indicating that these two genes may be regulated by waterlogging stress.
-
Keywords:
- Brassica napus /
- BnaMAP70 gene family /
- Waterlogging tolerance /
- Bioinformatics
-
甘蓝型油菜 (Brassica napus L.) 是我国重要的油料作物之一,并且是食用植物油和饲用蛋白的重要来源。长江中下游作为我国油菜种植主要区域,由于常年湿润多雨的气候和水稻 (Oryza sativa L.) -油菜轮作制度,使得油菜在苗期通常会遭受大面积的渍水胁迫,造成严重的经济损失[1, 2]。渍水胁迫可使土壤中的含氧量迅速降低,造成缺氧环境,从而导致植物根系活力降低、根毛减少等[3, 4]。甘蓝型油菜根部无法形成通气组织,渍水严重时可导致根系腐烂植株死亡[5, 6]。缺氧环境还会在植株内产生次生胁迫影响油菜的生长发育,如乙醛和乙醇毒害细胞[7]、内源激素合成受阻加速叶片的黄化衰老[8]、细胞结构受损等[9],导致油菜生长缓慢,产量下降[10, 11]。
全基因组关联分析表明,候选耐渍性相关基因主要编码激素响应蛋白、氧化胁迫和盐胁迫响应蛋白等[12]。RNA-Seq分析结果显示,油菜耐渍材料‘中双9号’和敏感材料‘GH01’淹水后差异表达的基因主要涉及细胞壁形成、环境胁迫响应及激素调控等[13],其中细胞骨架相关差异表达基因包括了微管相关蛋白 (Microtubule-associated proteins, MAPs) MAP70s基因家族成员MAP70-1和MAP70-4[14, 15]。微管作为细胞内物质运输、信号转导的重要通道,微管活动、微管相关蛋白的表达差异使得不同油菜品种表现出不同的耐渍性表型[16, 17]。但目前对甘蓝型油菜BnaMAP70s基因家族调控甘蓝型油菜耐渍性机理的研究还未见报道。
本研究通过生物信息学方法筛选甘蓝型油菜MAP70s基因家族成员,分析其与拟南芥 (Arabidopsis thaliana (L). Heynh.)、白菜 (Brassica rapa L.)、甘蓝 (Brassica oleracea L.) MAP70s基因的进化关系。利用qRT-PCR方法分析BnaMAP70-1和BnaMAP70-4基因在强耐渍甘蓝型油菜品种‘阳光2009’和敏感材料‘中双6号’中的转录水平。研究结果旨在为深入研究BnaMAP70s基因家族的生理功能、作用机制和培育甘蓝型油菜强耐渍性新品种提供参考依据。
1. 材料与方法
1.1 实验材料
渍水敏感性甘蓝型油菜品种‘中双6号’和强耐渍性品种‘阳光2009’均来自中国农业科学院油料作物研究所。
1.2 BnaMAP70s基因家族的鉴定及染色体定位分析
从TAIR (https://www.arabidopsis.org/)[18]中筛选出AtMAP70s基因家族成员。从甘蓝型油菜数据库BnPIR (http://cbi.hzau.edu.cn/bnapus/)[19]中下载‘中双11号’(‘ZS11’)的蛋白序列文件、基因组文件和基因注释文件。以AtMAP70s蛋白序列为查询序列,利用TBtools v1.095 [20]软件进行比对筛选。通过Pfam数据库 (https://pfam.xfam.org/search/) [21] 获取MAP70s蛋白的隐马尔可夫模型 (HMM model, PF07058)。以MAP70s的HMM模型为种子序列进行hmm 搜索[22] (https://www.ebi.ac.uk/)。并将两种方法获得的蛋白序列进行比对去重,利用NCBI的BlastP (BLAST: Basic Local Alignment Search Tool (nih.gov)) [23]、Uniport (https://www.uniprot.org/)、CD-search (https://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi) [24]分别进行蛋白注释信息、二级结构和保守结构域验证,对最终鉴定得到的BnaMAP70s蛋白成员进行重命名。分别利用Expasy (https://www.expasy.org/) [25]、WoLF PSORT (https://wolfpsort.hgc.jp/) [26]、TBtools v1.095软件进行理化性质分析、亚细胞定位和染色体定位预测。
1.3 MAP70s基因家族系统进化树构建和共线性分析
从Ensembl Plants (https://plants.ensembl.org/) [27]数据库下载甘蓝 (BOL)、白菜 (Brapa_1.0) 的蛋白序列文件和基因组文件,筛选白菜和甘蓝MAP70s基因家族成员。采用MEGA-X [28]软件基于Neighbor-Joining (邻接) 法构建系统进化树,iTOL (https://itol.embl.de/ ) [29]美化修饰进化树,TBtools v1.095软件进行共线性分析及可视化绘图。
1.4 BnaMAP70s家族基因结构、基序、保守结构域和顺式作用元件分析
分别利用GSDS(http://gsds.gao-lab.org/)[30]、MEME (https://meme-suite.org/meme/doc/meme.html) [31]、CD-search、PlantCare (https://bioinformatics.psb.ugent.be/webtools/plantcare/html/)[32]进行基因结构、保守基因(motif)、保守结构域和基因启动子上游2000 bp序列的顺式作用元件预测分析。
1.5 BnaMAP70s基因表达模式分析
从甘蓝型油菜转录组数据库BnTIR (http://yanglab.hzau.edu.cn/BnTIR/) [33]中获取BnaMAP70s在甘蓝型油菜不同部位、不同时期的转录水平,利用GraphPad Prism v8.0.2软件绘制基因表达量的热图。
1.6 渍水处理与qRT-PCR分析
植物种子于铺有两层湿润滤纸的培养皿中发芽,将长势一致的幼苗移栽到土壤中,置于恒温光照培养箱中,生长条件为 (25 ± 1) ℃,光照强度为1.3 × 103 Lux,光周期为16 h光照/8 h黑暗。待植株长至两片真叶时进行渍水处理 (水面高出土壤表面3 cm) 36 h,整株迅速置于液氮中速冻,于−80 ℃保存。
提取植株的总RNA,并反转录合成cDNA。采用NCBI (https://www.ncbi.nlm.nih.gov/) 的BlastP程序,对于从前人转录组分析数据中筛选得到的3个MAP70s相关基因Bra004053、Bra004279、Bra026184[14]进行同源序列比对,得到2个BnaMAP70s基因家族序列,利用Primer 5.0软件设计引物,以Actin为内参基因 (附表1
1 ),进行荧光定量检测,利用2−△△CT 法[34]进行基因表达的相对定量分析。2. 结果与分析
2.1 BnaMAP70s基因家族的鉴定及基因染色体定位
本研究从甘蓝型油菜‘ZS11’基因组中鉴定得到BnaMAP70s家族成员共19个,并依据其所属的MAP70s亚家族及其在染色体上的定位进行重命名 (附表2
1 )。理化性质分析结果表明,19个BnaMAP70基因编码的氨基酸数量为469 ~ 630;蛋白质相对分子质量为52505.48 ~ 70455.88 Da;蛋白质理论等电点为6.51 ~ 9.58;不稳定指数为47.52 ~ 58.59;平均亲水性为−0.883 ~ −0.724。19个BnaMAP70中有4个成员定位在叶绿体,2个成员定位在细胞质,11个成员定位在细胞核,2个成员定位在细胞质膜。蛋白质亚细胞定位预测结果显示,BnaMAP70s家族成员分布于细胞内的多个部位,与不同微管阵列作用部位具有一致性[35-37]。染色体定位分析发现 (附图1
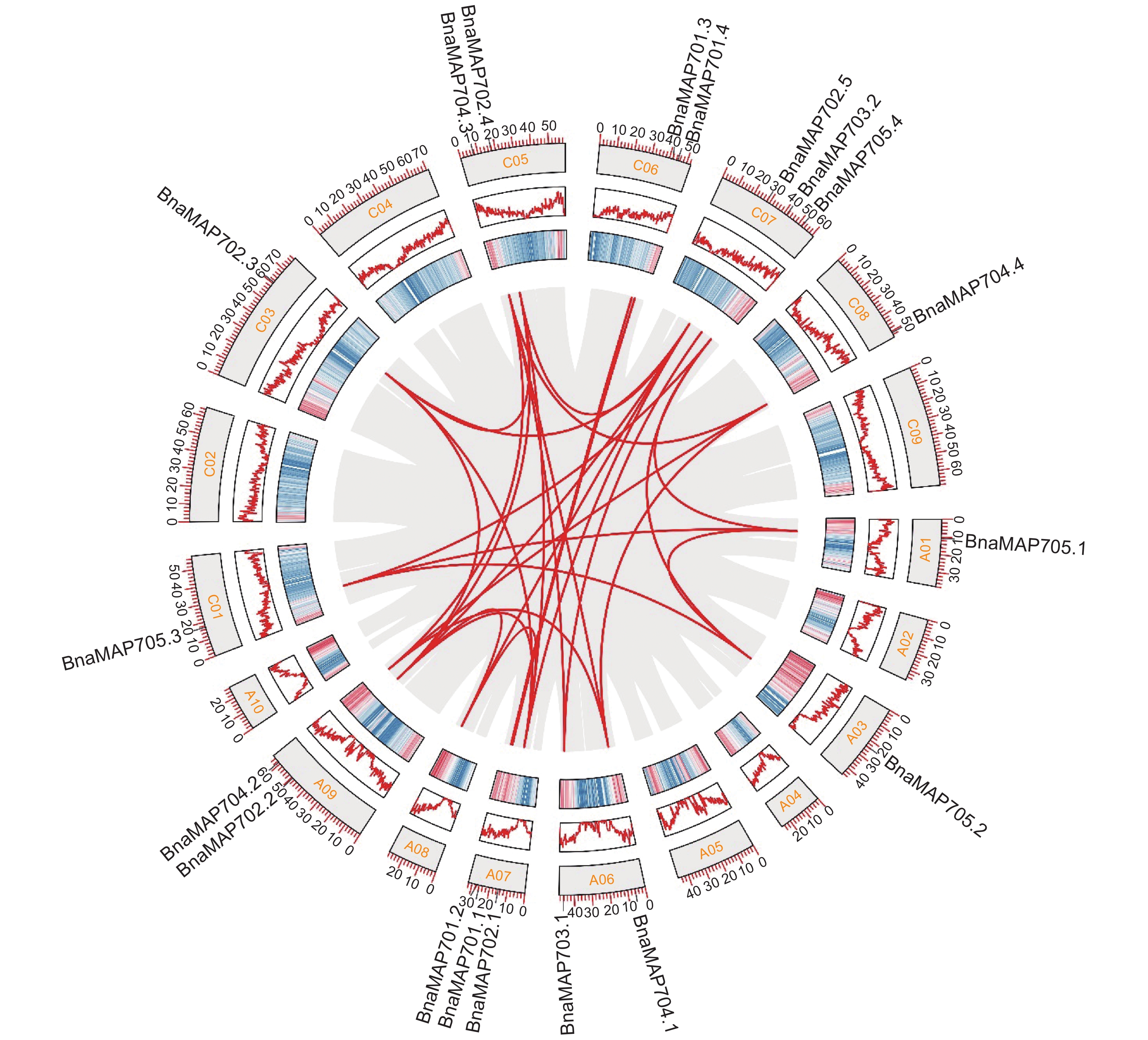
1 ),A01、A03、C01、C03、C08均分布1个BnaMAP70基因;A06、A09、C05、C06均分布2个BnaMAP70基因;A07、C07均分布3个BnaMAP70基因,且甘蓝型油菜MAP70s基因家族中未发现基因串联重复现象。2.2 MAP70s基因家族系统进化树构建和共线性分析
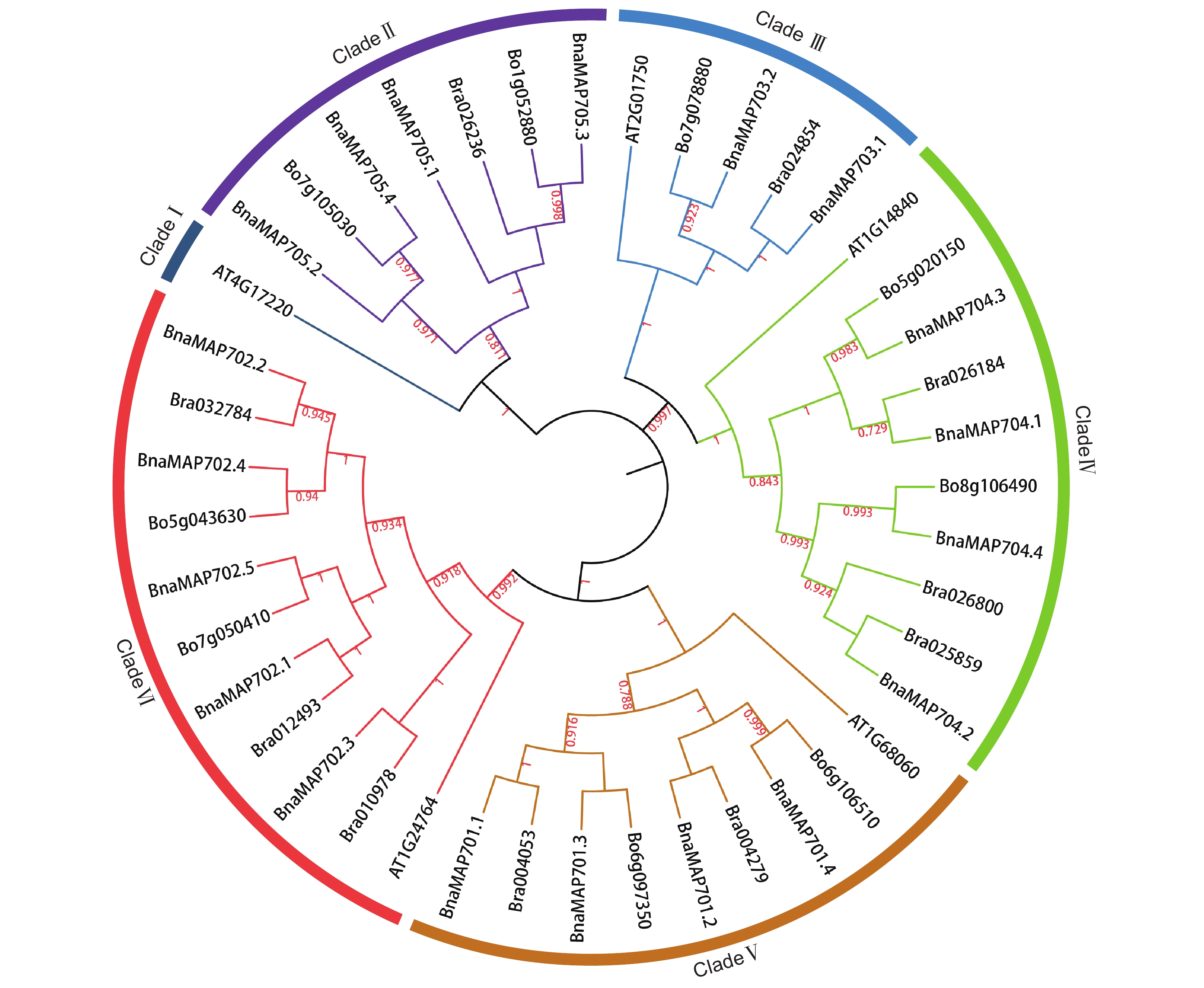
进化树分析结果显示,根据进化关系远近可将43个MAP70蛋白分为6个亚族 (图1)。其中,CladeⅡ含有BnaMAP705s亚家族所有成员 (BnaMAP705.1 ~ 705.4);CladeⅢ ~ CladeⅥ分别含有BnaMAP703s (BnaMAP703.1、BnaMAP703.2)、BnaMAP704s (BnaMAP704.1 ~ 704.4)、BnaMAP701s (BnaMAP701.1 ~ 701.4)、BnaMAP702s (BnaMAP702.1 ~ 702.5) 亚家族所有成员。甘蓝BoMAP70s、白菜BraMAP70s都含有5个亚族,且分别与不同的BnaMAP70s蛋白成员位于同一分支。拟南芥AtMAP70s含有5个亚族,其中CladeⅠ亚族仅有拟南芥AT4G17220一条蛋白序列,与其他AtMAP70s序列间差异较大。
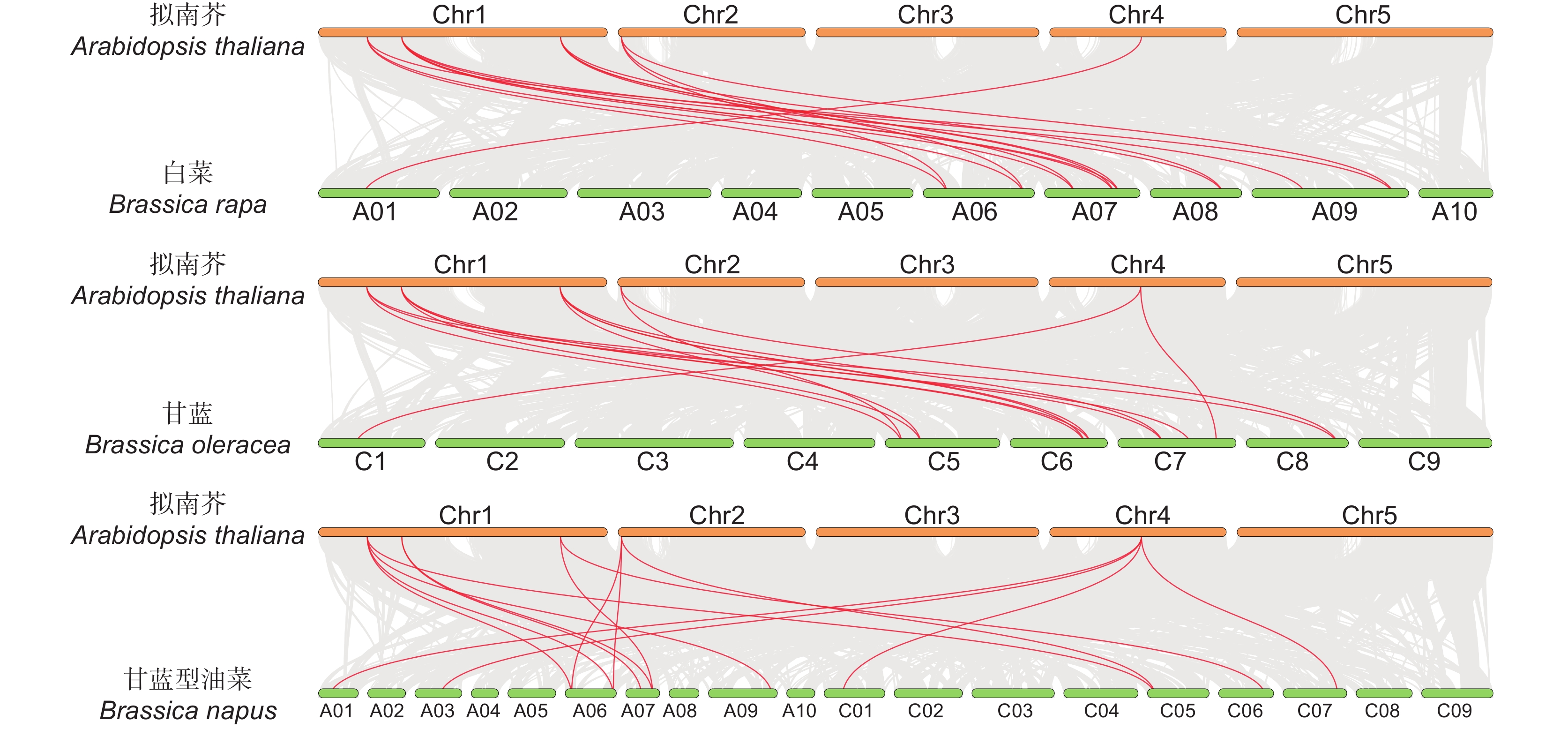
共线性分析结果表明 (图2),甘蓝型油菜具有20个BnaMAP70共线性位点,与鉴定得到的BnaMAP70s基因家族具有19个成员的结论不符,说明甘蓝型油菜在双二倍化过程中A08染色体上可能出现了基因拷贝的丢失(BnaA08T0224600ZS)。种间共线性分析发现 (图3),19个BnaMAP70基因中有11个基因与拟南芥存在共线性关系;BoMAP70s与BraMAP70s基因中都有9个基因与拟南芥存在共线性关系,我们认为这些存在共线性关系的MAP70s基因在进化过程中具有保守性,可能调控同一个性状。
2.3 BnaMAP70s家族基因结构和顺式作用元件分析
BnaMAP70s基因家族成员结构分析结果表明 (附图2
2 ),同一分支的亚家族成员间存在结构差异,如外显子数量为8 ~ 11个,UTR数量为0 ~ 4个。此外,内含子插入长度也不同,BnaMAP702.3内含子插入片段最长,使得其基因长度与其他成员具有明显差异,推测不同BnaMAP70s基因间功能的差异可能是由基因序列差异所导致。保守motif分析发现(附图32 ),所有成员都含有motif 1、2、9,表明这3个motif序列对于BnaMAP70s家族具有重要意义。此外BnaMAP703s、BnaMAP705s同一亚家族成员间含有的保守基序个数和编号一致 (分别为10个和9个),这一现象与不同成员间基因结构存在差异的现象一致。保守结构域分析结果显示 (附图4
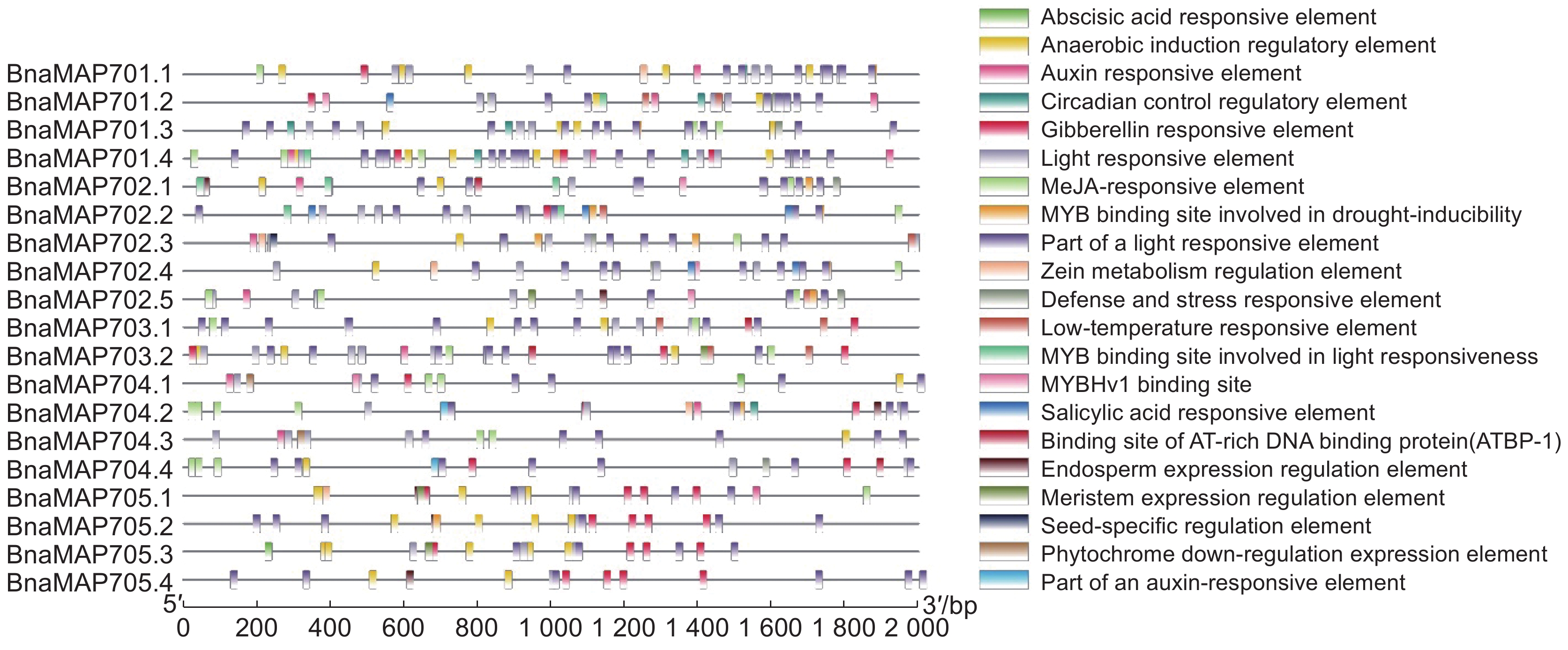
2 ),19个家族成员都含有MAP70和MAP70 superfamily结构域,除BnaMAP701.3和BnaMAP705s只含有MAP70 Superfamily结构域外,其他所有家族成员都含有SMC或SMC_Pork_A、SMC_Pork_B及其超家族结构域。已知SMC结构域的功能是参与分离染色体并维持染色体的结构,推测相关BnaMAP70s蛋白调控纺锤体微管阵列将染色体拉向细胞两级,促进细胞分裂。BnaMAP702.1和BnaMAP702.2含有PTZ00121结构域,已知该结构域具有黏附作用,可将两种不同蛋白家族的蛋白黏附在一起。BnaMAP701.2、BnaMAP704.1和BnaMAP704.2含有PRK03918结构域,该结构域主要功能是参与双链DNA的断裂修复,推测相关蛋白可能协助纺锤体微管阵列正确分离染色体并参与维持染色体的稳定。BnaMAP703s和BnaMAP704.1 ~ 704.3还含有功能未知的Pneumo_PspA结构域,该类蛋白存在于细菌中,可能具有重要功能。BnaMAP70s家族顺式作用元件可以大致分为3类 (图4),第1类是光响应顺式作用元件,包括ACE、GT1-motif、Box4等;第2类是激素类响应元件,包括生长素、赤霉素、水杨酸、茉莉酸甲酯、脱落酸响应元件;第3类是逆境胁迫响应元件,包括MYB结合位点、低温和厌氧响应元件。在响应逆境胁迫相关的所有顺式作用元件中,厌氧诱导响应元件为最大的一类顺式作用元件,19个BnaMAP70s基因家族成员中除BnaMAP702.2、BnaMAP702.5、BnaMAP704.2外,其他16个成员都含有该元件。表明BnaMAP70s参与细胞内多种抗逆境胁迫反应,尤其是渍水胁迫反应,并受大量激素调节。
2.4 BnaMAP70s表达模式分析
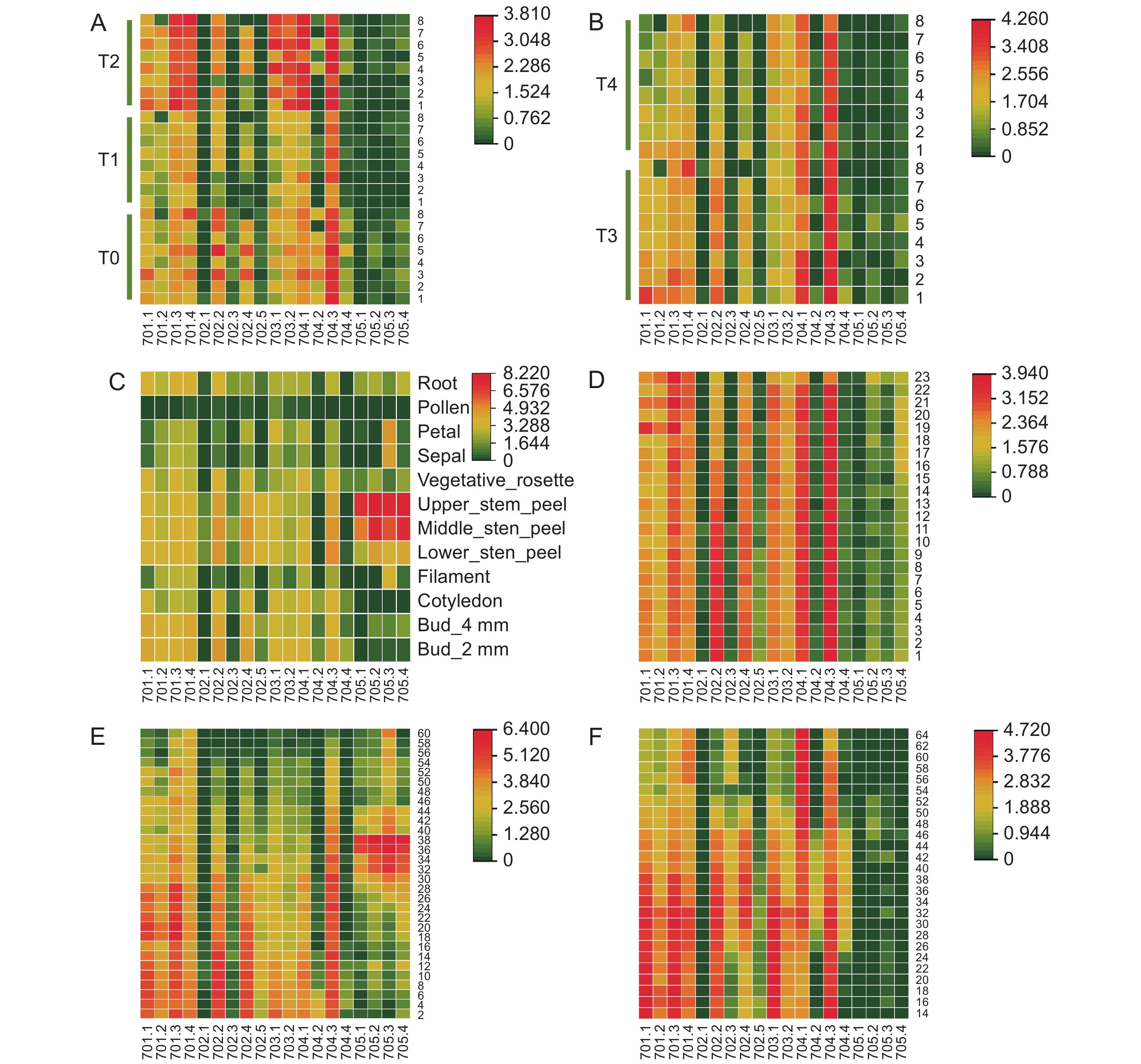
BnaMAP70s在不同甘蓝型油菜品种 (‘Quinta’、‘Tapidor’、‘Shengli’、‘Zheyou’、‘Gangan’、‘ZS11’、‘Westar’、‘NO2127’) 叶片的5个生长时期 (T0 ~ T4) 中转录水平的热图分析结果显示 (图5:A),大部分基因在T1 (播种后54 d) 时期的转录水平最低,在T2 (播种后82 d) 和T3 时期(播种后115 d) 的转录水平显著增加达到最大。BnaMAP701.3、BnaMAP701.4、BnaMAP703.2、BnaMAP704.1、BnaMAP704.3在不同品种叶片的不同发育时期,都具有较高的转录水平。BnaMAP704.2和BnaMAP704.4在T0 (播种后24 d) 时期有少量表达,在其他时期低表达甚至不表达。而BnaMAP702.1、BnaMAP702.3、BnaMAP702.5、BnaMAP705s在叶片整个发育时期的表达量都较低甚至不表达。总的来说,BnaMAP70s在不同油菜品种、不同发育时期的基因表达模式不同,表现出基因表达的特异性、品种特异性和表达时期特异性。
![]() 图 5 BnaMAP70s转录水平分析701.1~705.4 分别对应基因 BnaMAP701.1~BnaMAP705.4。A、B:不同甘蓝型油菜 (1:‘Quinta’;2:‘Tapidor’;3:‘Shengli’;4:‘Zheyou’;5:‘Gangan’;6:‘ZS11’;7:‘Westar’;8:‘NO2127’) 叶片中 BnaMAP70s 基因转录水平 (T0~T5分别为播种后第24、54、82、115、147 天);C:BnaMAP70s 在 ‘ZS11’ 不同部位的基因转录水平;D:BnaMAP70s 在 ‘ZS11’ 不同时期叶片中的基因转录水平 (1~23为第1~23片叶);E:BnaMAP70s 在 ‘ZS11’ 不同时期角果中的基因转录水平 (2~60为开花后第2~60 天);F:BnaMAP70s 在 ‘ZS11’ 不同时期种子中的基因转录水平 (14~64为开花后第 14~64 天)。Figure 5. Transcriptional levels of BnaMAP70s701.1-705.4 in the heat map correspond to the genes BnaMAP701.1-BnaMAP705.4 respectively. A,B: Transcription levels of BnaMAP70s gene in leaves (T0~T5: 24, 54, 82, 115, 147 day after sowing) of different B. napus (1: ‘Quinta’; 2: ‘Tapidor’; 3: ‘Shengli’; 4: ‘Zheyou’; 5: ‘Gangan’; 6: ‘ZS11’; 7: ‘Westar’; 8: ‘NO2127’); C: Gene transcription levels of BnaMAP70s in different parts of ‘ZS11’; D: Gene transcription levels of BnaMAP70s in leaves at different periods of ‘ZS11’(1~23: leaf 1-23); E: Gene transcription levels of BnaMAP70s in silique at different periods of ‘ZS11’(2~60: 2-60 day after flowering); F: Gene transcription levels of BnaMAP70s in seed at different periods of ‘ZS11’(14~64: 14-64 day after flowering).
图 5 BnaMAP70s转录水平分析701.1~705.4 分别对应基因 BnaMAP701.1~BnaMAP705.4。A、B:不同甘蓝型油菜 (1:‘Quinta’;2:‘Tapidor’;3:‘Shengli’;4:‘Zheyou’;5:‘Gangan’;6:‘ZS11’;7:‘Westar’;8:‘NO2127’) 叶片中 BnaMAP70s 基因转录水平 (T0~T5分别为播种后第24、54、82、115、147 天);C:BnaMAP70s 在 ‘ZS11’ 不同部位的基因转录水平;D:BnaMAP70s 在 ‘ZS11’ 不同时期叶片中的基因转录水平 (1~23为第1~23片叶);E:BnaMAP70s 在 ‘ZS11’ 不同时期角果中的基因转录水平 (2~60为开花后第2~60 天);F:BnaMAP70s 在 ‘ZS11’ 不同时期种子中的基因转录水平 (14~64为开花后第 14~64 天)。Figure 5. Transcriptional levels of BnaMAP70s701.1-705.4 in the heat map correspond to the genes BnaMAP701.1-BnaMAP705.4 respectively. A,B: Transcription levels of BnaMAP70s gene in leaves (T0~T5: 24, 54, 82, 115, 147 day after sowing) of different B. napus (1: ‘Quinta’; 2: ‘Tapidor’; 3: ‘Shengli’; 4: ‘Zheyou’; 5: ‘Gangan’; 6: ‘ZS11’; 7: ‘Westar’; 8: ‘NO2127’); C: Gene transcription levels of BnaMAP70s in different parts of ‘ZS11’; D: Gene transcription levels of BnaMAP70s in leaves at different periods of ‘ZS11’(1~23: leaf 1-23); E: Gene transcription levels of BnaMAP70s in silique at different periods of ‘ZS11’(2~60: 2-60 day after flowering); F: Gene transcription levels of BnaMAP70s in seed at different periods of ‘ZS11’(14~64: 14-64 day after flowering).BnaMAP70s基因家族在‘ZS11’不同组织部位中的表达特征表明 (图5:B ~ D),BnaMAP701s和BnaMAP703s两个亚家族成员在根、子叶、叶片、花蕾、早期角果中均表现出高的转录水平。BnaMAP702.2、BnaMAP702.4在根、子叶、叶、花蕾、早期角果、种子中具有高的转录水平;BnaMAP702.1和BnaMAP702.3在所有油菜部位中转录水平都较低;BnaMAP702.5在角果、茎皮中具有较高转录水平。BnaMAP704s亚家族中,BnaMAP704.1和BnaMAP704.3在子叶、花蕾、角果、种子中具有较高表达量;BnaMAP704.2和BnaMAP704.4仅在种子 (28 ~ 44 DAF) 中具有较高基因表达量。BnaMAP705s亚家族成员仅在角果 (26 ~ 44 DAF) 和茎皮中具有高表达量,推测BnaMAP705s亚家族成员可能在茎的生长及角果发育成熟方面具有重要作用。
2.5 基因表达分析
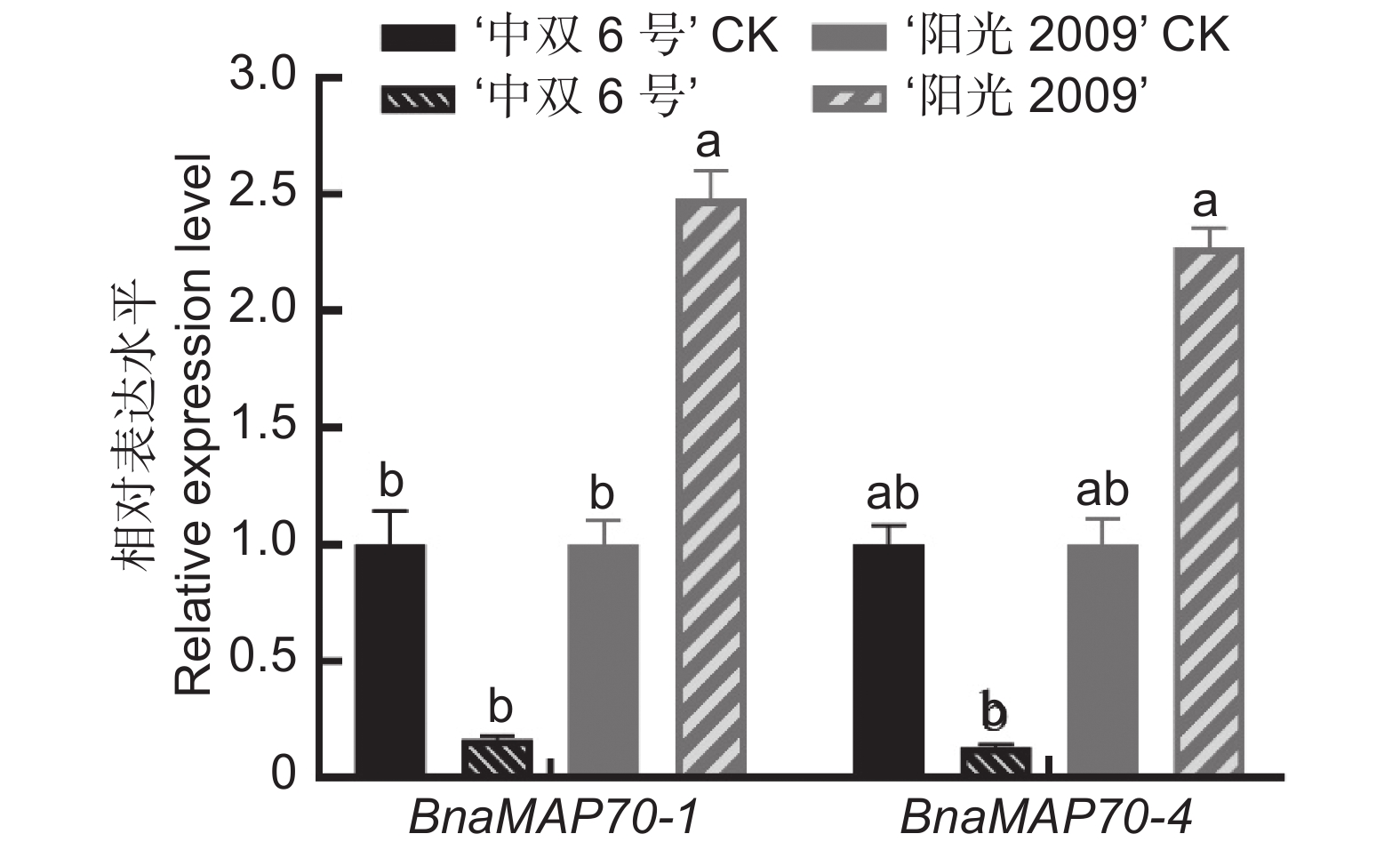
基因表达分析发现 (图6),耐渍性较弱的品种‘中双6号’经渍水处理后,BnaMAP70-1与BnaMAP70-4的基因相对转录水平都低于对照组,表明‘中双6号’经渍水胁迫下调了基因的转录水平。在强耐渍性油菜品种‘阳光2009’中,渍水胁迫上调了两个基因的相对表达量。此外BnaMAP70-1的转录水平均高于BnaMAP70-4,这一现象同基因表达量热图中油菜根部BnaMAP704s的基因转录水平低于BnaMAP701s的结果一致。
3. 讨论
微管相关蛋白通过调控微管阵列和稳定微管结构参与细胞内重要的生理活动[38],多种微管相关蛋白的基因结构和功能都已得到鉴定[39],但甘蓝型油菜BnaMAP70s的相关研究却未见报道。本研究在甘蓝型油菜‘ZS11’全基因组中共鉴定到19个BnaMAP70家族成员。系统进化分析结果显示,MAP701s ~ MAP704s的进化关系更近,而与MAP705s的进化关系较远,这一现象与前人[40]研究结果一致。通过比较拟南芥MAP70s基因家族基因在其他3个物种基因组中的拷贝数可知,MAP70s基因在甘蓝型油菜 (19条)、白菜 (10条)、甘蓝基因组 (9条) 中的拷贝数都有所增加,表明所有MAP70s基因在芸薹属 (Brassica) 多倍化过程中都发生了基因增加的现象。甘蓝型油菜由白菜和甘蓝经种间杂交后双二倍化形成,理论上甘蓝型油菜中BnaMAP70s基因个数为甘蓝和白菜中MAP70s基因数之和,然而甘蓝型油菜种内共线性分析发现,BnaMAP70s在基因进化过程中发生了基因拷贝的丢失 (BnaA08T0224600ZS);进一步的种间共线性分析结果表明,甘蓝型油菜19个BnaMAP70基因中仅存在11个共线性位点,其中5个亚家族中只有BnaMAP705s亚家族所有成员存在共线性位点,结合系统进化树、基因结构、保守基序和保守结构域的分析结果,我们认为BnaMAP705s亚家族各成员可能具有相同的蛋白功能。总的来说,BnaMAP705s亚家族进化过程高度保守,在甘蓝型油菜的进化过程中具有重要作用;其他亚家族为了适应甘蓝型油菜细胞内多种生命活动及生长发育的需要,推测亚家族不同成员间可能出现了蛋白功能的差异[41]。
甘蓝型油菜BnaMAP70s顺式作用元件分析结果表明,大部分BnaMAP70s成员启动子上游存在厌氧及渍水胁迫响应元件。不定根的形成是植株适应渍水胁迫的重要方式之一[42],Bao等[43]的研究也发现AtMAP70-5通过调节内胚层皮质微管阵列促进侧根的形态发生,推测MAP70-5是促进不定根生成的重要蛋白因子。有研究[44]进一步发现MAP70-5与皮质微管阵列的结合通过整合并传递相关信息促进侧根的生成,认为生长素信号是调控MAP70-5促进侧根形成的关键因子。因此,推测渍水胁迫下生长素参与调控MAP70-5促进不定根的生成。渍水胁迫还导致甘蓝型油菜根部木质素沉积,出现明显木质化,降低了根部的水分传导率,提高了水分和氧气运输效率,增强了植物的适应性[45-47]。Pesquet 等[48, 49]的研究表明,MAP70对木质部次生细胞壁形成的导管形状及导管模式具有重要调控作用,其中MAP70-5是MAP70s家族中唯一存在于木质部的成员,AtMAP70-5与AtMAP70-1对木质部次级细胞壁的准确定位至关重要。本研究中,BnaMAP70-1、BnaMAP70-4在渍水胁迫下出现差异表达,进一步证明BnaMAP70s受渍水胁迫的调控。综上所述,本研究认为BnaMAP70s在甘蓝型油菜抗渍水胁迫方面发挥重要功能,并受到相关植物激素的调控。
1 1~ 3)如需查阅附件内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。2 1 ~ 3)如需查阅附件内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。 -
图 5 BnaMAP70s转录水平分析
701.1~705.4 分别对应基因 BnaMAP701.1~BnaMAP705.4。A、B:不同甘蓝型油菜 (1:‘Quinta’;2:‘Tapidor’;3:‘Shengli’;4:‘Zheyou’;5:‘Gangan’;6:‘ZS11’;7:‘Westar’;8:‘NO2127’) 叶片中 BnaMAP70s 基因转录水平 (T0~T5分别为播种后第24、54、82、115、147 天);C:BnaMAP70s 在 ‘ZS11’ 不同部位的基因转录水平;D:BnaMAP70s 在 ‘ZS11’ 不同时期叶片中的基因转录水平 (1~23为第1~23片叶);E:BnaMAP70s 在 ‘ZS11’ 不同时期角果中的基因转录水平 (2~60为开花后第2~60 天);F:BnaMAP70s 在 ‘ZS11’ 不同时期种子中的基因转录水平 (14~64为开花后第 14~64 天)。
Figure 5. Transcriptional levels of BnaMAP70s
701.1-705.4 in the heat map correspond to the genes BnaMAP701.1-BnaMAP705.4 respectively. A,B: Transcription levels of BnaMAP70s gene in leaves (T0~T5: 24, 54, 82, 115, 147 day after sowing) of different B. napus (1: ‘Quinta’; 2: ‘Tapidor’; 3: ‘Shengli’; 4: ‘Zheyou’; 5: ‘Gangan’; 6: ‘ZS11’; 7: ‘Westar’; 8: ‘NO2127’); C: Gene transcription levels of BnaMAP70s in different parts of ‘ZS11’; D: Gene transcription levels of BnaMAP70s in leaves at different periods of ‘ZS11’(1~23: leaf 1-23); E: Gene transcription levels of BnaMAP70s in silique at different periods of ‘ZS11’(2~60: 2-60 day after flowering); F: Gene transcription levels of BnaMAP70s in seed at different periods of ‘ZS11’(14~64: 14-64 day after flowering).
-
[1] Fan XL,Zhang ZS,Gao HY,Yang C,Liu MJ,et al. Photoinhibition-like damage to the photosynthetic apparatus in plant leaves induced by submergence treatment in the dark[J]. PLoS One,2014,9 (2):e89067. doi: 10.1371/journal.pone.0089067
[2] Sundgren TK,Uhlen AK,Lillemo M,Briese C,Wojciechowski T. Rapid seedling establishment and a narrow root stele promotes waterlogging tolerance in spring wheat[J]. J Plant Physiol,2018,227:45−55. doi: 10.1016/j.jplph.2018.04.010
[3] Lynch JP. Root phenes that reduce the metabolic costs of soil exploration:opportunities for 21st century agriculture[J]. Plant Cell Environ,2015,38 (9):1775−1784. doi: 10.1111/pce.12451
[4] Ploschuk RA,Miralles DJ,Colmer TD,Ploschuk EL,Striker GG. Waterlogging of winter crops at early and late stages:impacts on leaf physiology,growth and yield[J]. Front Plant Sci,2018,9:1863. doi: 10.3389/fpls.2018.01863
[5] Ambros S,Kotewitsch M,Wittig PR,Bammer B,Mustroph A. Transcriptional response of two Brassica napus cultivars to short-term hypoxia in the root zone[J]. Front Plant Sci,2022,13:897673. doi: 10.3389/fpls.2022.897673
[6] Yamauchi T,Colmer TD,Pedersen O,Nakazono M. Regulation of root traits for internal aeration and tolerance to soil waterlogging-flooding stress[J]. Plant Physiol,2018,176 (2):1118−1130. doi: 10.1104/pp.17.01157
[7] Sauter M. Root responses to flooding[J]. Curr Opin Plant Biol,2013,16 (3):282−286. doi: 10.1016/j.pbi.2013.03.013
[8] Gibbs DJ,Lee SC,Isa N,Gramuglia S,Fukao T,et al. Homeostatic response to hypoxia is regulated by the N-end rule pathway in plants[J]. Nature,2011,479 (7373):415−418. doi: 10.1038/nature10534
[9] Tong C,Hill CB,Zhou GF,Zhang XQ,Jia Y,Li CD. Opportunities for improving waterlogging tolerance in cereal crops-physiological traits and genetic mechanisms[J]. Plants (Basel)
,2021,10 (8):1560. doi: 10.3390/plants10081560 [10] 马海清,刘清云,高立兵,胡志文,张清香,等. 油菜初花期淹水胁迫对产量及构成因子的影响[J]. 中国农业文摘-农业工程,2020,32(6):77−80. doi: 10.3969/j.issn.1002-5103.2020.06.029 [11] 俞建河,王本来,曹秀清,沈涛. 淹水时期与天数对油菜生长性状和产量的影响[J]. 安徽农业科学,2021,49(14):184−187. doi: 10.3969/j.issn.0517-6611.2021.14.049 Yu JH,Wang BL,Cao XQ,Shen T. Effects of flooding period and days on the growth traits and yield of rapeseed[J]. Journal of Anhui Agricultural Sciences,2021,49 (14):184−187. doi: 10.3969/j.issn.0517-6611.2021.14.049
[12] 李阳阳,荆蓉蓉,吕蓉蓉,石鹏程,李欣,等. 甘蓝型油菜湿害胁迫响应性状的全基因组关联分析及候选基因预测[J]. 作物学报,2019,45(12):1806−1821. Li YY,Jing RR,LÜ RR,Shi PC,Li X,et al. Genome-wide association analysis and candidate genes prediction of waterlogging-responding traits in Brassica napus L.[J]. Acta Agronomica Sinica,2019,45 (12):1806−1821.
[13] 徐明月. 甘蓝型油菜发芽期耐渍相关基因的筛选[D]. 北京: 中国农业科学院, 2014: 31. [14] Zou XL,Zeng L,Lu GY,Cheng Y,Xu JS,Zhang XK. Comparison of transcriptomes undergoing waterlogging at the seedling stage between tolerant and sensitive varieties of Brassica napus L.[J]. J Integr Agr,2015,14 (9):1723−1734. doi: 10.1016/S2095-3119(15)61138-8
[15] Zou XL,Tan XY,Hu CW,Zeng L,Lu GP,et al. The transcriptome of Brassica napus L. roots under waterlogging at the seedling stage[J]. Int J Mol Sci,2013,14 (2):2637−2651. doi: 10.3390/ijms14022637
[16] Li JJ,Iqbal S,Zhang YT,Chen YH,Tan ZD,et al. Transcriptome analysis reveals genes of flooding-tolerant and flooding-sensitive rapeseeds differentially respond to flooding at the germination stage[J]. Plants (Basel)
,2021,10 (4):693. doi: 10.3390/plants10040693 [17] 李继军. 油菜响应苗期渍害的动态过程和遗传基础[D]. 武汉: 华中农业大学, 2021: 17. [18] Poole RL. The TAIR database[J]. Methods Mol Biol,2007,406:179−212.
[19] Song JM,Liu DX,Xie WZ,Yang ZQ,Guo L,et al. BnPIR:Brassica napus pan-genome information resource for 1689 accessions[J]. Plant Biotechnol J,2021,19 (3):412−414. doi: 10.1111/pbi.13491
[20] Chen CJ,Chen H,Zhang Y,Thomas HR,Frank MH,et al. TBtools:an integrative toolkit developed for interactive analyses of big biological data[J]. Mol Plant,2020,13 (8):1194−1202. doi: 10.1016/j.molp.2020.06.009
[21] Mistry J,Chuguransky S,Williams L,Qureshi M,Salazar GA,et al. Pfam:The protein families database in 2021[J]. Nucleic Acids Res,2021,49 (D1):D412−D419. doi: 10.1093/nar/gkaa913
[22] McWilliam H,Li WZ,Uludag M,Squizzato S,Park YM,et al. Analysis tool web services from the EMBL-EBI[J]. Nucleic Acids Res,2013,41:W597−W600. doi: 10.1093/nar/gkt376
[23] Johnson M,Zaretskaya I,Raytselis Y,Merezhuk Y,McGinnis S,Madden TL. NCBI BLAST:a better web interface[J]. Nucleic Acids Res,2008,36 (W):W5−W9.
[24] Yang MZ,Derbyshire MK,Yamashita RA,Marchler-Bauer A. NCBI's conserved domain database and tools for protein domain analysis[J]. Curr Protoc Bioinformatics,2020,69 (1):e90.
[25] Gasteiger E,Gattiker A,Hoogland C,Ivanyi I,Appel RD,Bairoch A. ExPASy:the proteomics server for in-depth protein knowledge and analysis[J]. Nucleic Acids Res,2003,31 (13):3784−3788. doi: 10.1093/nar/gkg563
[26] Horton P,Park KJ,Obayashi T,Fujita N,Harada H,et al. WoLF PSORT:protein localization predictor[J]. Nucleic Acids Res,2007,35 (W):W585−W587.
[27] Bolser DM, Staines DM, Perry E, Kersey PJ. Ensembl plants: integrating tools for visualizing, mining, and analyzing plant genomic data[M]//Van Dijk ADJ, ed. Plant Genomics Databases. New York: Humana Press, 2017, 1533: 1-31.
[28] Hall BG. Building phylogenetic trees from molecular data with MEGA[J]. Mol Biol Evol,2013,30 (5):1229−1235. doi: 10.1093/molbev/mst012
[29] Letunic I,Bork P. Interactive Tree Of Life (iTOL) v5:an online tool for phylogenetic tree display and annotation[J]. Nucleic Acids Res,2021,49 (W1):W293−W296. doi: 10.1093/nar/gkab301
[30] Hu B,Jin JP,Guo AY,Zhang H,Luo JC,Gao G. GSDS 2.0:an upgraded gene feature visualization server[J]. Bioinformatics,2015,31 (8):1296−1297. doi: 10.1093/bioinformatics/btu817
[31] Bailey TL,Boden M,Buske FA,Frith M,Grant CE,et al. MEME SUITE:tools for motif discovery and searching[J]. Nucleic Acids Res,2009,37 (W):W202−W208.
[32] Lescot M,Déhais P,Thijs G,Marchal K,Moreau Y,et al. PlantCARE,a database of plant cis-acting regulatory elements and a portal to tools for in silico analysis of promoter sequences[J]. Nucleic Acids Res,2002,30 (1):325−327. doi: 10.1093/nar/30.1.325
[33] Liu DX,Yu LQ,Wei LL,Yu PG,Wang J,et al. BnTIR:an online transcriptome platform for exploring RNA-seq libraries for oil crop Brassica napus[J]. Plant Biotechnol J,2021,19 (10):1895−1897. doi: 10.1111/pbi.13665
[34] Livak KJ,Schmittgen TD. Analysis of relative gene expression data using real-time quantitative PCR and the
2−ΔΔCT Method[J]. Methods,2001,25 (4):402−408. doi: 10.1006/meth.2001.1262[35] Lee YRJ,Liu B. Microtubule nucleation for the assembly of acentrosomal microtubule arrays in plant cells[J]. New Phytol,2019,222 (4):1705−1718. doi: 10.1111/nph.15705
[36] Goodson HV,Jonasson EM. Microtubules and microtubule-associated proteins[J]. Cold Spring Harb Perspect Biol,2018,10 (6):a022608. doi: 10.1101/cshperspect.a022608
[37] Struk S,Dhonukshe P. MAPs:cellular navigators for microtubule array orientations in Arabidopsis[J]. Plant Cell Rep,2014,33 (1):1−21. doi: 10.1007/s00299-013-1486-2
[38] Brouhard GJ,Rice LM. The contribution of αβ-tubulin curvature to microtubule dynamics[J]. J Cell Biol,2014,207 (3):323−334. doi: 10.1083/jcb.201407095
[39] Gardiner J. The evolution and diversification of plant microtubule-associated proteins[J]. Plant J,2013,75 (2):219−229. doi: 10.1111/tpj.12189
[40] Korolev AV,Chan J,Naldrett MJ,Doonan JH,Lloyd CW. Identification of a novel family of 70 kDa microtubule-associated proteins in Arabidopsis cells[J]. Plant J,2005,42 (4):547−555. doi: 10.1111/j.1365-313X.2005.02393.x
[41] Panchy N,Lehti-Shiu M,Shiu SH. Evolution of gene duplication in plants[J]. Plant Physiol,2016,171 (4):2294−2316. doi: 10.1104/pp.16.00523
[42] Zaman MS,Malik AI,Kaur P,Erskine W. Waterlogging tolerance of pea at germination[J]. J Agro Crop Sci,2018,204 (2):155−164. doi: 10.1111/jac.12230
[43] Bao ZR, Guo Y, Deng YL, Zang JZ, Zhang JH, et al. The microtubule-associated protein SlMAP70 interacts with SlIQD21 and regulates fruit shape formation in tomato[J/OL]. BioRxiv, 2022. doi: 10.1101/2022.08.08.503161.
[44] Stöckle D,Reyes-Hernández BJ,Barro AV,Nenadić M,Winter Z,et al. Microtubule-based perception of mechanical conflicts controls plant organ morphogenesis[J]. Sci Adv,2022,8 (6):eabm4974. doi: 10.1126/sciadv.abm4974
[45] Arduini I,Kokubun M,Licausi F. Editorial:crop response to waterlogging[J]. Front Plant Sci,2019,10:1578. doi: 10.3389/fpls.2019.01578
[46] Liu MM,Tan XF,Sun XH,Zwiazek JJ. Properties of root water transport in canola (Brassica napus) subjected to waterlogging at the seedling,flowering and podding growth stages[J]. Plant and Soil,2020,454 (1):431−445.
[47] Ryser P,Gill HK,Byrne CJ. Constraints of root response to waterlogging in Alisma triviale[J]. Plant Soil,2011,343 (1):247−260.
[48] Pesquet E,Korolev AV,Calder G,Lloyd CW. Mechanisms for shaping,orienting,positioning and patterning plant secondary cell walls[J]. Plant Signal Behav,2011,6 (6):843−849. doi: 10.4161/psb.6.6.15202
[49] Pesquet E,Korolev AV,Calder G,Lloyd CW. The microtubule-associated protein AtMAP70-5 regulates secondary wall patterning in Arabidopsis wood cells[J]. Curr Biol,2010,20 (8):744−749. doi: 10.1016/j.cub.2010.02.057
-
期刊类型引用(2)
1. 谢伶俐,李永铃,许本波,张学昆. 油菜耐渍机理解析及遗传改良研究进展. 作物学报. 2025(02): 287-300 .  百度学术
百度学术
2. 蒋晓晗,聂笑一. 甘蓝型油菜基因组缺失变异检测研究. 粮油与饲料科技. 2024(06): 199-201 .  百度学术
百度学术
其他类型引用(0)
-
其他相关附件
-
PDF格式
黄郢附件 点击下载(1015KB)
-



 下载:
下载: