Analysis of fruit quality and sensory evaluation of 36 kiwifruit (Actinidia) germplasm accessions
-
摘要:
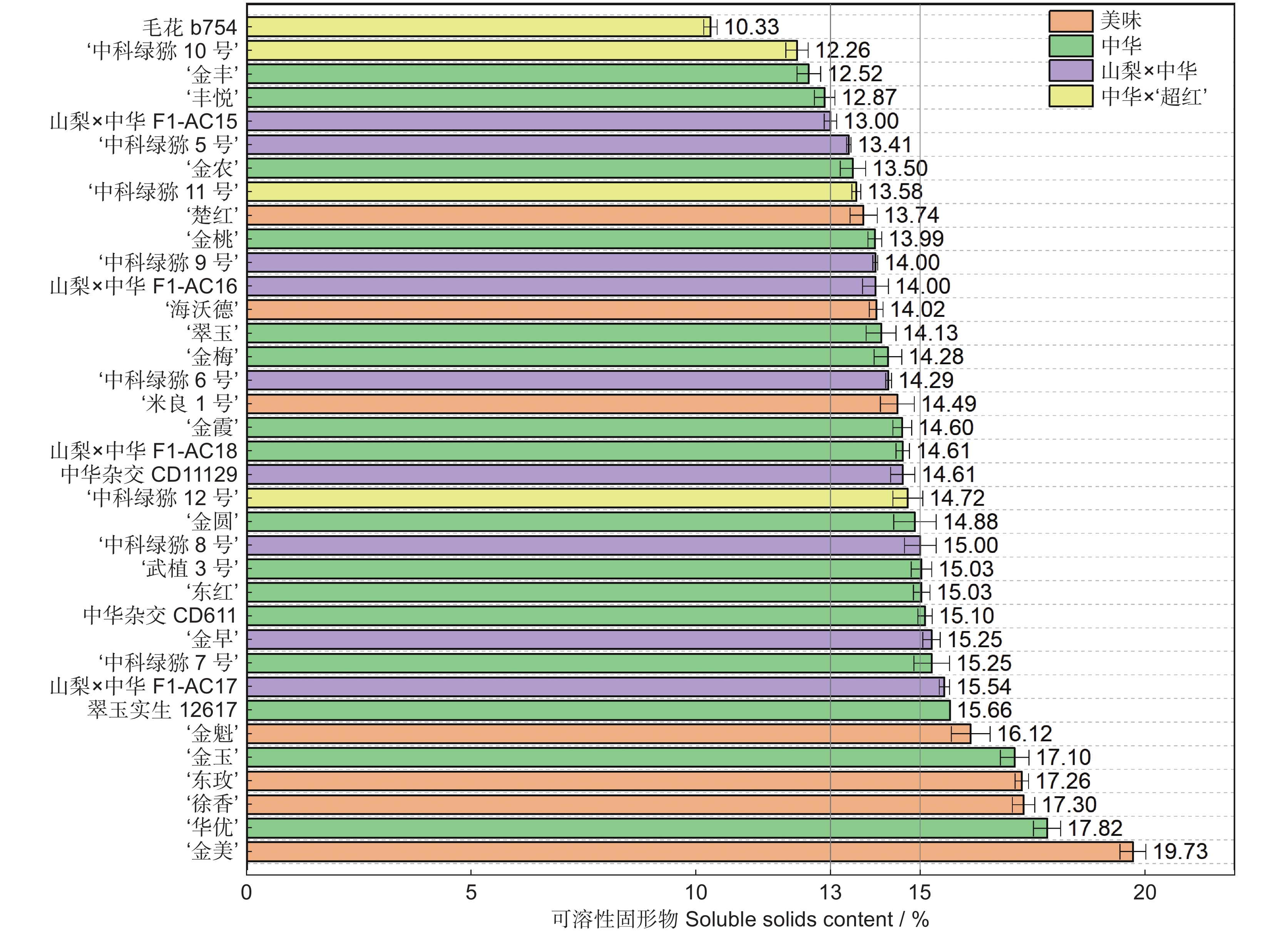
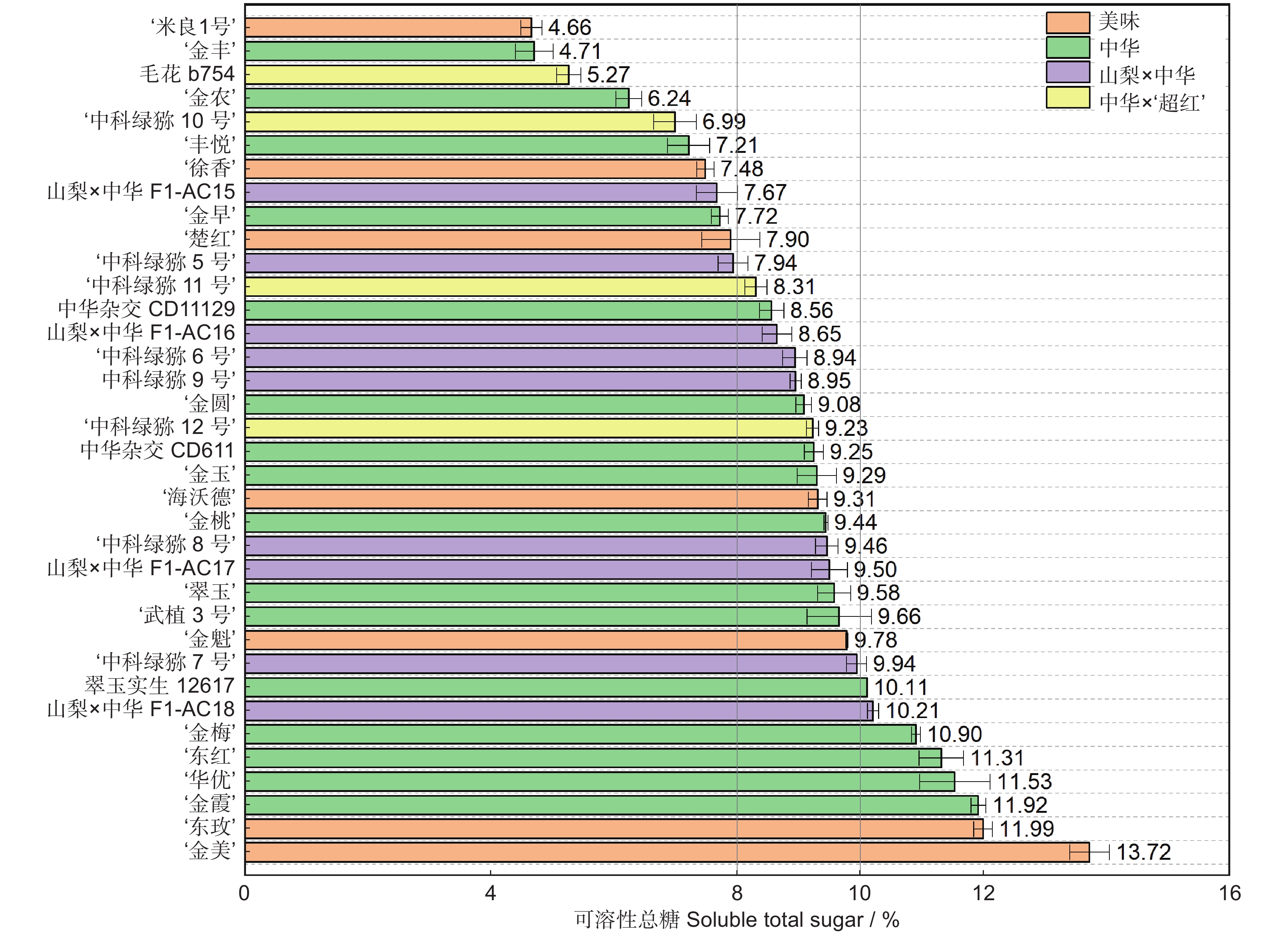
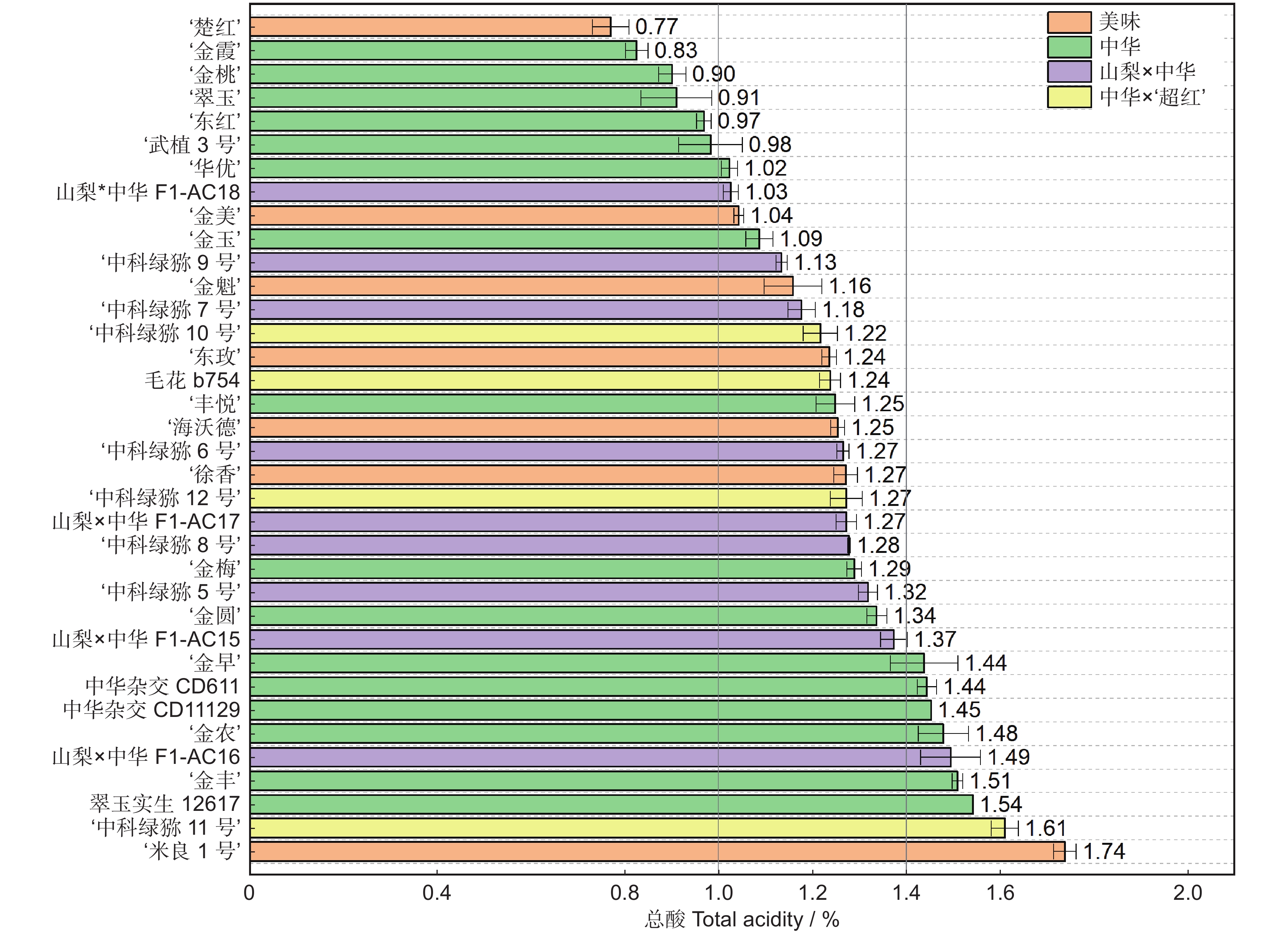
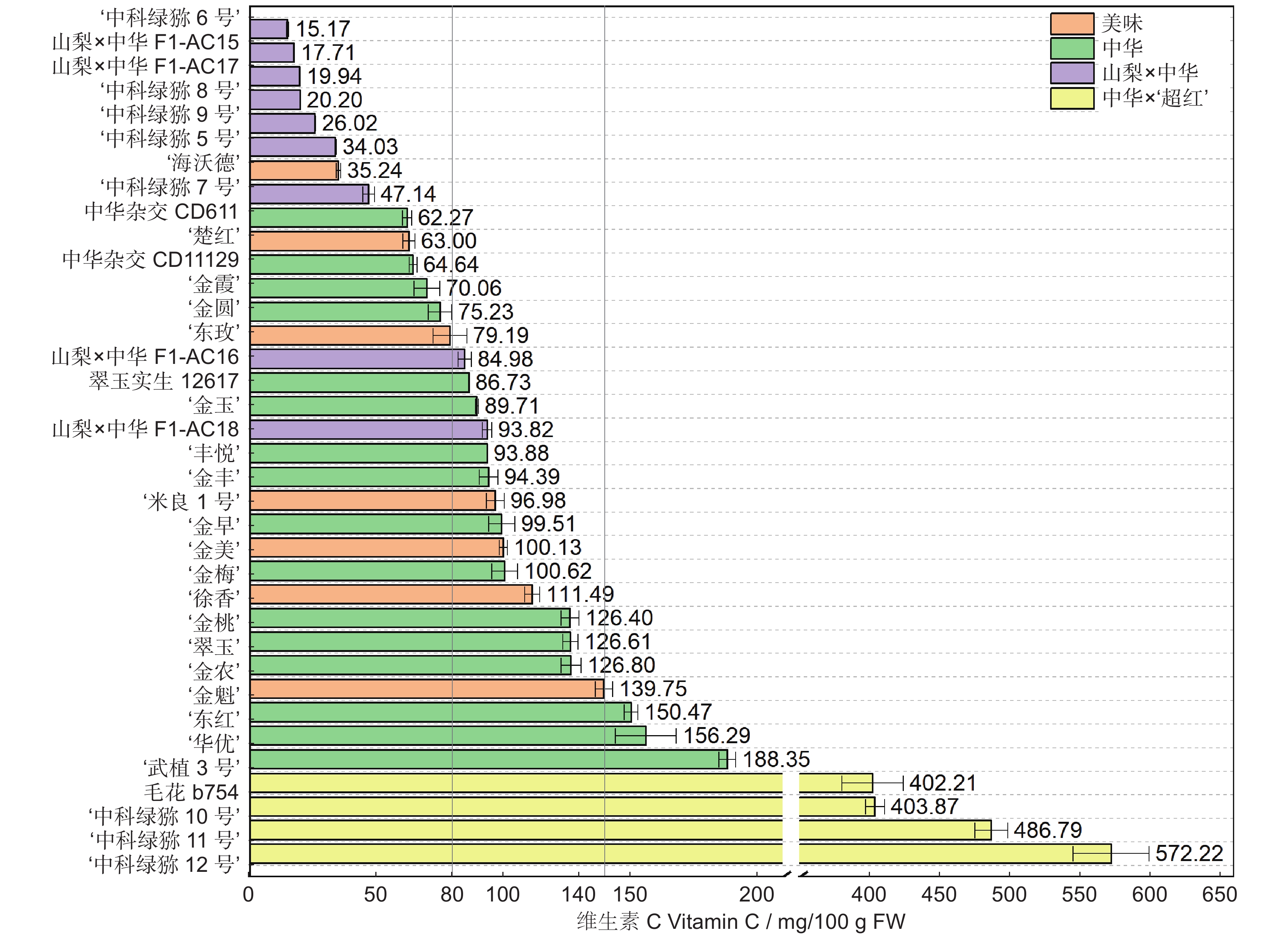
以湖北省丹江口市同一猕猴桃(Actinidia)资源圃内的36份不同种质,包括:7个美味猕猴桃(变种)(A. chinensis var. deliciosa (A. Chev.) A. Chev.)、16个中华猕猴桃(原变种)(A. chinensis var. chinensis Planch.)、9个山梨猕猴桃(A. rufa (Sieb. & Zucc.) Planch. ex Mi.) × 中华猕猴桃和4个中华猕猴桃 × ‘超红’猕猴桃(A. eriantha Benth. × A. chinensis var. chinensis Planch.)的果实为研究对象,在可溶性固形物 ≥ 7.0%时采收,测定果实采收成熟度和软熟内在品质指标,并分析果实感官评价及其与内在品质的相关性。结果显示,36份猕猴桃种质果实品质性状表现出明显的差异性,尤其是单果重和维生素C(Vc)含量,其变异系数分别为43.61%和103.16%。这与山梨 × 中华及中华 × ‘超红’种类有关,两个种类均为小果型(< 45 g);前者Vc含量最低(39.89 mg/100 g),后者最高(466.27 mg/100 g)。36份软熟果实样本中可溶性固形物、可溶性总糖和总酸的平均值分别为14.70%、8.96%和1.24%,其中可溶性固形物在美味种类中的平均值最高,最低为中华 × ‘超红’种类。果实感官评价在不同样本之间也表现出明显的差异性,就种类而言,山梨 × 中华的感官评价质量略高于其他种类。整体喜好度与风味喜好度、甜度紧密正相关(Pearson r ≥ 0.94),而与酸度有一定程度的负相关(r = −0.53)。可溶性固形物、可溶性总糖与整体喜好度的相关性明显高于总酸,但Vc与整体喜好度则无相关性。
Abstract:Thirty-six different accessions of kiwifruit (Actinidia), including seven Actinidia chinensis var. deliciosa (A. Chev.) A. Chev., 16 A. chinensis var chinensis Planch., nine A. rufa (Sieb. & Zucc.) Planch. ex Mi. × A. chinensis var. chinensis Planch., and four A. chinensis var. chinensis × ‘Chaohong’ (A. eriantha Benth. × A. chinensis var. chinensis Planch.) grown in a same kiwifruit germplasm garden in Danjiangkou City, Hubei Province, were used as study materials. The fruits were harvested once soluble solids content (SSC) reached 7.0%. Fruit maturity at harvest and internal quality of ripe fruit were measured, and sensory evaluation and correlation with internal qualities were also analyzed. Results indicated significant differences in fruit quality traits among the 36 accessions, particularly fruit fresh weight and vitamin C (Vc) content, which had the highest coefficients of variation (43.61% and 103.16%, respectively). The significant variations were associated with samples from the A. rufa × A. chinensis and A. chinensis × ‘Chaohong’ groups. These two groups had small fruit size (< 45 g of average fresh weight), with the former having the lowest level of Vc (39.89 mg/100 g) and the latter having the highest (466.27 mg/100 g). Average SSC, soluble sugar, and total acidity of the 36 kiwifruit accessions were 14.70%, 8.96%, and 1.24%, respectively, and average SSC was highest in the A. chinensis var. deliciosa group and lowest in the A. chinensis × ‘Chaohong’ group. The sensory evaluation scores also revealed significant differences among samples, with the A. rufa × A. chinensis group showing the best sensory qualities. Overall liking was highly positively correlated with flavor liking and sweetness (Pearson r ≥ 0.94), but negatively correlated with acidity (r = −0.53). Overall liking revealed a higher correlation with sweetness indices (SSC and soluble sugar) than the acidity index (total acidity), but no clear correlation with Vc.
-
Keywords:
- Actinidia /
- Fruit quality /
- Sensory evaluation /
- Correlation
-
异戊烯基转移酶(Prenyltransferases,PTs)是生物体内负责催化异戊烯基化反应的一大类酶,其催化反应需要异戊烯基供体和受体。供体通常是异戊二烯焦磷酸(XPP,X代表不同长度的异戊烯基链),如二甲基烯丙基焦磷酸(Dimethylallyl diphosphate,DMAPP,C5)、香叶基焦磷酸(Geranyl diphosphate,GPP,C10)、法尼基焦磷酸(Farnesyl diphosphate,FPP,C15)和香叶基香叶基焦磷酸(Geranylgeranyl diphosphate,GGPP,C20)等[1](图1:A)。供体XPP上的二磷酸基团裂解产生异戊烯基末端的反应性碳正离子中间体,这种碳正离子与受体反应,发生类似于Friedel-Crafts芳香亲电取代机制的异戊烯基化[2](图1:B)。
![]() 图 1 UbiA异戊烯基转移酶的分类、一般催化机制和供体的结构式A:异戊二烯焦磷酸结构式;B:UbiA异戊烯基转移酶的一般催化机制;C:异戊烯基转移酶的分类。Figure 1. Classification and general catalytic mechanism of UbiA prenyltransferases and structural formula of isoprenyl diphosphatesA: Structural formula of isoprenyl diphosphates; B: General catalytic mechanism of UbiA superfamily prenyltransferases; C: Classification of prenyltransferases.
图 1 UbiA异戊烯基转移酶的分类、一般催化机制和供体的结构式A:异戊二烯焦磷酸结构式;B:UbiA异戊烯基转移酶的一般催化机制;C:异戊烯基转移酶的分类。Figure 1. Classification and general catalytic mechanism of UbiA prenyltransferases and structural formula of isoprenyl diphosphatesA: Structural formula of isoprenyl diphosphates; B: General catalytic mechanism of UbiA superfamily prenyltransferases; C: Classification of prenyltransferases.根据受体的不同,通常将异戊烯基转移酶分为以下4类:(1)以异戊二烯焦磷酸(Isopentenyl pyrophosphate,IPP)为受体的异戊烯基焦磷酸合酶(Prenyl diphosphate synthases),参与单萜(Monoterpenoids)、倍半萜(Sesquiterpenes)、二萜(Diterpenes)和类胡萝卜素(Carotenoids)等化合物的生物合成;(2)以芳香族化合物为受体的芳香族异戊烯基转移酶(Aromatic prenyltransferases),催化芳香族化合物与异戊烯基形成C-C(或C-O)键,生成具有生物学功能的化合物;(3)以多肽为受体的蛋白质异戊烯基转移酶(Protein prenyltransferases),它们在真核生物蛋白质翻译后修饰中起着重要的作用;(4)以核苷酸为受体的tRNA异戊烯基转移酶(tRNA prenyltransferases),参与tRNA的生物合成与修饰[1, 3](图1:C)。
芳香族异戊烯基转移酶广泛存在于植物、动物、真菌和细菌中,根据蛋白序列同源性及空间构象的不同,可将其分为两大类:UbiA膜结合型芳香族异戊烯基转移酶和ABBA型可溶性芳香族异戊烯基转移酶,后者主要来自于细菌和真菌[4](图1:C)。1972年,Young等[5]从大肠杆菌中分离鉴定第一个UbiA的基因,推测其功能为催化对羟基苯甲酸(p-hydroxybenzoic acid,PHB)与异戊烯基生成3-辛异戊烯基-4-羟基苯甲酸。此后,在植物和人类中发现了一系列具有与UbiA类似的功能,均为膜结合型蛋白,至少包含一个富含天冬氨酸的基序(如NQxxDxxxD),用于结合异戊二烯焦磷酸,它们的活性完全依赖于Mg2 + 或类似的二价阳离子[6],因此把具有这些特点的酶组成的家族称为UbiA异戊烯基转移酶超家族(UbiA superfamily)。目前已报道的植物来源的芳香族异戊烯基转移酶基因都属于UbiA超家族。
异戊烯基化修饰带来了植物代谢物的多样性,芳香环上的异戊烯基化的位置不同,异戊烯基链的长度不同,以及异戊烯基基团的进一步修饰,如环化和羟基化,导致产生大量结构类型各异的异戊烯基化合物[7]。这些代谢产物在许多植物的生长发育和抗病中发挥着不可或缺的作用[8, 9]。异戊烯基化修饰可以增加这些化合物的亲脂性,使化合物分子与生物膜的亲和力增强,从而可增加其生物利用度、改善药物代谢和药物动力学特性[10]。植物中的芳香族异戊烯基转移酶为膜结合型蛋白,基因克隆和外源表达具有一定的难度,且一般具有严格的底物特异性和空间位点专一性(一般只能催化一种类型的底物,且邻位有OH的位点更容易异戊烯基化)[11, 12],因此研究进展比较缓慢。根据底物的不同,植物芳香族异戊烯基转移酶可分为初生代谢相关的异戊烯基转移酶(Primary metabolite-related prenyltransferases,PMPTs)和与次生代谢相关的异戊烯基转移酶(也称为多酚类异戊烯基转移酶,Polyphenolic prenyltransferase,PHPTs)两大类(图1:C)。
本文系统介绍了植物中两类UbiA PTs,包括PMPTs和PHPTs,重点归纳了已鉴定功能的57个催化次生代谢物(类黄酮、香豆素、二苯乙烯等)的PHPTs的底物选择性和催化特点,分析了它们与PMPTs的系统发育关系,并对异戊烯基转移酶基因的挖掘策略,以及利用微生物代谢工程定向合成活性异戊烯基化合物的应用前景进行了展望。
1. 初生代谢物合成相关的异戊烯基转移酶
1.1 对羟基苯甲酸异戊烯转移酶(PPT)
对羟基苯甲酸异戊烯基转移酶(p-hydroxybenzoate polyprenyltransferase,PPT)以对羟基苯甲酸(PHB)为底物,将不同长度的异戊烯基基团(通常是30~50个碳)转移到PHB上合成泛醌(Ubiquinone,UQ)(呼吸链中的电子载体)[3]。拟南芥(Arabidopsis thaliana (L.) Heynh.)中的AtPPT1和水稻(Oryza sativa L.)的OsPPT1a,均可接受多种供体,如AtPPT1供体可以是茄尼基焦磷酸(Solanesyl diphosphate,SDP,C45)和GPP(C10),而底物严格为PHB[13, 14](附图1:A
1 )。在紫草(Lithospermum erythrorhizon Sieb. et Zucc.)中发现有些成员(LePGT-1和LePGT-2)以PHB为底物,仅可以GPP(C10)为供体,最终合成紫草素(Shikonin)(附图1:A)[15, 16]。此外,在软紫草(Arnebia euchroma(Royle)Johnst.)中鉴定的AePGT、AePGT4和AePGT6具有类似的功能[17]。
1.2 尿黑酸异戊烯基转移酶(HGPT)
尿黑酸异戊烯转移酶(Homogentisate prenyltransferase,HGPT)以尿黑酸(Homogentisate acid,HGA)为底物,称为尿黑酸异戊烯转移酶家族(HGPT family),根据异戊烯基供体的不同分为3种类型:尿黑酸植基转移酶(Homogentisate phytyltransferase,HPT,VTE2-1),供体为植基焦磷酸(Phytyl diphosphate,PDP,C20),合成生育酚(Tocopherol)的前体物质[18]。尿黑酸香叶基香叶基转移酶(Homogentisate geranylgeranyl transferase,HGGT),供体为GGPP(C20),合成生育三烯酚(Tocotrienol)的前体物质[19]。尿黑酸茄尼基转移酶(Homogentisate solanesyltransferase,HST,VTE2-2),供体为SDP(C45),合成质体醌(Plastoquinone)的前体[20](附图1:B)。
生育酚和生育三烯酚统称为维生素E。动物和人体不能合成维生素E,只能通过植物性食物摄入。因此鉴定农作物中参与维生素E生物合成的基因进行转基因改造提高维生素E含量也是目前代谢工程研究的热点[21]。
1.3 叶绿素合成酶(CHLSYN / ATG4)
叶绿素是高等植物进行光合作用的主要色素,叶绿素合成酶(Chlorophyll synthases,CHLSYN,ATG4)可以催化脱植基叶绿素(Chlorophyllide)与PDP(C20)反应直接生成叶绿素(Chlorophyll)(附图1:C),也可以通过间接的方式,先催化脱植基叶绿素与GGPP(C20)反应生成香叶基香叶基叶绿素(Chlorophyllgg),再在香叶基香叶基焦磷酸还原酶的作用下生成叶绿素[22]。
1.4 亚铁血红素O合成酶(COX10)
亚铁血红素A(Heme A)属于细胞色素a。亚铁血红素O合成酶(Heme O synthase,HOS,COX10)催化FPP(C15)与亚铁血红素B(Heme B,血红素IX,Protoheme IX)反应,生成亚铁血红素O(Heme O),随后再生成亚铁血红素A(附图1:D)[23]。
1.5 DHNA植基转移酶(ABC4)
维生素K1(Vitamin K1)又称叶绿醌(Phylloquinone),主要存在于陆生植物和藻类中。DHNA植基转移酶(1,4-Dihydroxy-2-napthoic acid phytyltransferase,Aberrant chloroplast development 4,ABC4)催化PDP(C20)与1,4-二羟基-2-萘甲酸(1,4-Dihydroxy-2-napthoic acid,DHNA)反应,生成Demethylphylloquinone,进一步在甲基转移酶(MT)的作用下生成叶绿醌(附图1:E)[24]。
2. 次生代谢物合成相关的异戊烯基转移酶
2.1 类黄酮异戊烯基转移酶(FPT)
异戊烯基类黄酮是一类重要的植物次生代谢产物,其特点是在不同结构的黄酮类化合物母核的C-6、C-8、C-3′或C-5′位置上存在异戊烯基侧链,少数在C-7、C-2′位(紫檀烷类和查耳酮的取代位置相似,但是C编号不同)(图2)。该类化合物主要分布在豆科、桑科、大麻科、小檗科、菊科、芸香科和伞形科等植物中。异戊烯基类黄酮具有抗炎、抗菌、抗骨质疏松、抗肿瘤和雌激素样作用等活性,且异戊烯基侧链的不同结合位点、数量及结构类型决定了其生物活性的多样性[25, 26]。
类黄酮异戊烯基转移酶(Flavonoid prenyltransferase,FPT)是最早发现的植物PHPHs。植物中已鉴定出1000多种异戊烯基类黄酮[27-41],但迄今为止从植物中鉴定出的类黄酮异戊烯基转移酶只有23个,大部分具有严格的底物和供体特异性,催化活性依赖二价阳离子(表1)。在豆科中,以苦参(Sophora flavescens Alt.)和大豆(Glycine max (L.) Merr.)中发现的基因居多。2008年,从苦参中克隆得到了第一个植物类黄酮异戊烯基转移酶基因SfN8DT-1,该基因编码的蛋白催化DMAPP与柚皮素(Naringenin)结合,生成8-异戊烯基柚皮素(8-Prenylnaringenin)(附图2:A
2 )。此外,该酶可催化甘草素(Liquiritigenin)和橙皮素(Hesperetin)发生异戊烯基化反应,但表现出对二氢黄酮和DMAPP严格的底物和供体特异性[7]。Chen等[28]从苦参悬浮细胞培养液中鉴定出SfFPT,可催化多种结构类型的类黄酮底物(二氢黄酮、二氢查尔酮、二氢黄酮醇和黄酮),但对(2S)-二氢黄酮具有严格的立体异构特异性。表 1 植物类黄酮异戊烯基转移酶的催化特性Table 1. Catalytic properties of flavonoid prenyltransferases in plants物种名称
Species name蛋白名称
Protein name底物类型
Substrate type底物名称
Substrate name异戊烯基供体
Prenyl donor异戊烯基取代位点
Prenyl substitution site二价阳离子
Divalent cation参考文献
References苦参
Sophora flavescens Alt.SfN8DT-1 二氢黄酮 Liquiritigenin>Naringenin>
HesperetinDMAPP A环C-8位 Mg2 + [7] SfiLDT 查尔酮 Isoliquiritigenin DMAPP 未知 Mg2 + [33] SfG6DT 异黄酮 Genistein>Biochanina DMAPP、GPP1、FPP1 A环C-6位 Mg2 + >Ni2 + >
Mn2 + >Ca2 +[33] SfFPT 二氢查尔酮 Phloretin DMAPP、GPP2 A环C-3'位 Mg2 + >Ba2 + >Ca2 + >Fe2 + >Co2 + >Cu2 + >Zn2 + >Mn2 + [28] 二氢黄酮 Eriodictyol>Naringenin>
Pinocembrin>Liquiritigenin>
Hesperetin>Isosakuranetin>
Steppogenin>Tsugafolin>
SakuranetinA环C-8位 黄酮 Chrysin A环C-8位 二氢黄酮醇 Taxifolin A环C-8位 大豆
Glycine max (L.) Merr.GmG4DT 紫檀烷 Glycinol>Maackiain DMAPP A环C-4位 Mg2 + >Mn2 + >Co2 + [30] GmG2DT 紫檀烷 Glycinol DMAPP A环C-2位 Mg2 + >Mn2 + [29] GmPT01 紫檀烷 Glycinol DMAPP A环C-2位 Mg2 + [31] GmIDT1 异黄酮 Daidzein>Genistein DMAPP B环 Mg2 + >Mn2 + [29] GmIDT2 异黄酮 Daidzein≈Genistein DMAPP A环 Mg2 + >Mn2 + [29] GmIDT3 异黄酮 Daidzein、Genistein DMAPP 未知 Mg2 + [31] 白羽扇豆
Lupinus albus L.LaPT1 异黄酮 2-Hydroxygenistein>
GenisteinDMAPP B环C-3'位 Mg2 + >Mn2 + >Ni2 + >Co2 + >Zn2 + >Ca2 + [34] LaPT2 黄酮醇 Kaempferol>Kaempferide>Quercetin>Galangin>
Fesitin>MorinDMAPP A环C-8位 Mg2 + [12] 二氢黄酮 Naringenin DMAPP 未知 甘草
Glycyrrhiza uralensis Fisch.GuA6DT 黄酮 Apigenin>Chrysin>
Diosmtin>Luteolin>
Norartocarpetin>
ChrysoeroilDMAPP、GPP1 A环C-6位 Mg2 + >Mn2 + >Zn2 + >Fe2 + >Co2 + >Ca2 + >Ba2 + [11] GuILDT 查尔酮 2',4'-Dihydroxychalcone>
Isoliquiritigenin>
2,4,2',4'-Tetrahydro-xychalcone>
NaringeninchalconeDMAPP A环C-3'位 Mg2 + >Co2 + >Ni2 + >Fe2 + >Ba2 + >Mn2 + >Ca2 + [35] 百脉根
Lotus japonicus L.LjG6DT 异黄酮 Genistein DMAPP A环C-6位 Mg2 + >Co2 + >Mn2 + >Ca2 + >Zn2 + >Fe2 + [36] 补骨脂
Psoralea corylifolia (L.) Medik.PcM4DT 紫檀烷 Maackiain>3-Hydroxy-9-methoxypterocarpan DMAPP A环C-4位 Mg2 + >Mn2 + >Co2 + >Fe2 + >Ba2 + >Sr2 + >Ca2 + >Sn2 + >Ni2 + >Zn2 + [37] 桑
Morus alba L.MaIDT 查尔酮 Isoliquiritigenin>
2',4'-Dihydroxychalcone>
2,4,2',4'-Tetrahydroxychalcone>
ButeinDMAPP、GPP1 A环C-3'位 Mg2 + >Ba2 + >Ca2 + >Mn2 + >Fe2 + >Ni2 + [32] 异黄酮 Genistein>2'-Hydroxygenistein A环C-6位 黄酮 Apigenin A环C-6位 柘树
Cudrania tricuspidata (Carr.) Bur.CtIDT 查尔酮 Isoliquiritigenin>
2,4,2',4'-Tetrahydroxychalcone>
2',4'-Dihydroxychalcone>
ButeinDMAPP、GPP1 A环C-3'位 Mg2 + >Mn2 + >Ca2 + >Fe2 + >Ba2 + [32] 异黄酮 2'-Hydroxygenistein>
GenisteinA环C-6位 大麻
Cannabis sativa L.CsPT3 黄酮 Chrysoeriol>Apigenin DMAPP、GPP A环C-6位 Mg2 + [38] CsPT8 黄酮 Apigenin DMAPP 未知 Mg2 + [38] 啤酒花
Humulus lupulus L.HlPT-1 查尔酮 Naringenin chalcone DMAPP A环C-3'位 Mg2 + [39] 柔毛淫羊藿
Epimedium pubescens Maxim.EpPT8 黄酮醇 Kaempferol> Quercetin DMAPP A环C-8位 Mg2 + [40] 黄酮 Apigenin 箭叶淫羊藿
Epimedium sagittatum (Sieb. et Zucc.) Maxim.EsPT2 黄酮醇 Kaempferol>Kaempferide DMAPP A环C-8位 Mg2 + [41] 二氢黄酮 Naringenin 注:“>”用于表示对底物的催化活性顺序;1 研究只证明提供了该供体与最适底物发生异戊烯基化反应;2 GPP作为供体时,SfFPT仅催化pinocembrin,isosakuranetin和naringenin发生异戊烯基化反应。 Notes: “>” indicates order of catalytic activity to the substrate; 1 Prenylation of the donor with an optimal substrate is demonstrated; 2 SfFPT only catalyzed prenylation of pinocembrin, isosakuranetin, and naringenin when GPP was used as the prenyl donor. 大豆中的异黄酮类有一半以上具有异戊烯基取代,被认为是诱导型的植物防御素(Phytoalexins),如大豆抗毒素(Glyceollins)。GmG4DT和GmG2DT分别催化DMAPP与(−)-glycinol的C-2位和C-4位发生异戊烯基化反应,GmG4DT催化生成Glyceolin Ⅰ和Glyceollin Ⅵ的前体化合物4-dimethylallylglycinol,GmG2DT催化生成Glyceollin Ⅱ、Glyceollin Ⅲ和Glyceollin Ⅳ的前体化合物2-Dimethylallylglycino[29-31]。
桑(Morus alba L.)中的MaIDT和柘树(Cudrania tricuspidata (Carr.) Bur.)中的CtIDT是首次鉴定出来的非豆科FPTs,二者均可催化4种查尔酮的C-3′和两种异黄酮(Genistein和2′-Hydroxygenistein)的C-6位发生异戊烯基取代。而且发现MaIDT更偏向于查尔酮的异戊烯基化,而CtIDT更偏向于异黄酮的异戊烯基化[32]。
目前从植物中克隆并鉴定出的FPTs,大部分只能催化一种类型的类黄酮发生异戊烯基化反应,虽然SfFPT、MaIDT、CtIDT、LaPT2、EpPT8和EsPT2可催化两种及以上类型的类黄酮底物,但都对其中一种类黄酮结构催化活性强。大部分FPTs只可接受DMAPP为异戊烯基供体,少数可以接受GPP或FPP作为供体,但对DMAPP的催化效率最高。FPTs对不同结构的黄酮类化合物母核催化位点具有特异性,一种FPT只能催化底物的一个位点。
2.2 香豆素异戊烯基转移酶(CPT)
香豆素(Coumarin)广泛分布于植物中,在豆科、伞形科、桑科和芸香科尤为普遍[42]。根据其结构,可分为简单香豆素、呋喃香豆素、吡喃香豆素、双香豆素等。其中呋喃香豆素和吡喃香豆素为简单香豆素母核上C-6或C-8位的异戊烯基与7位酚羟基(7-OH)环合成呋喃或吡喃环,吡喃香豆素保留二甲基取代,呋喃香豆素后续又脱掉3个C。呋喃香豆素较为常见,具有抗肿瘤、抗氧化以及抗炎镇痛等多种药理活性[43]。
催化香豆素异戊烯基化反应的酶(Coumarins prenyltransferase,CPT)中最常见的是伞形酮异戊烯基转移酶(Umbelliferone dimethylallyltransferase,UDT),如伞形科欧芹(Petroselinum crispum (Mill.) Hill)中的PcPT,催化DMAPP转移到伞形酮的C-6和C-8位分别生成脱甲基软木花椒素(Demethylsuberosin,DMS)和欧芹酚(Osthenol),可进一步生成线型香豆素和角型香豆素[44](附图2:B);芸香科的柠檬(Citrus limon Burm. (L.) Burm. F.)中鉴定出的ClPT1只接受GPP为异戊烯基供体,催化伞形酮的C-8位 [45]。桑科的无花果(Ficus carica L.)中发现的FcPT1只接受DMAPP为异戊烯基供体,催化伞形酮的C-6位[46](表2)。
表 2 植物中香豆素异戊烯基转移酶的催化特性Table 2. Catalytic properties of coumarin prenyltransferases in plants物种名称
Species
name蛋白名称
Protein name底物名称
Substrate name异戊烯基
供体
Prenyl donor异戊烯基取代位点
Prenyl substitution
site二价阳离子
Divalent cation参考文献
References欧芹Petroselinum crispum (Mill.) Hill PcPT Umbelliferone DMAPP C-6位>C-8位 Mg2 + [44] 欧防风Pastinaca sativa L. PsPT1 Umbelliferone DMAPP C-6位>C-8位 Mg2 + [42] PsPT2 Umbelliferone DMAPP C-8位>C-6位 Mg2 + [42] 柠檬Citrus limon (L.) Burm. F. ClPT1 Umbelliferone>Esculetin>5,7-hydroxycoumarin
>5-Methoxy-7-hydroxycoumarinGPP C-8位 Mg2 + [45] 无花果Ficus carica L. FcPT1 Umbelliferone DMAPP C-6位 Mg2 + [46] 5-Methoxy-7-hydroxycoumarin DMAPP 未知 Mg2 + 葡萄柚Citrus paradisi Macf. CpPT1 5,7-Dihydroxycoumarin, 8-Hydroxybergapten 5-Hydroxy-7-methoxycoumarin, Bergaptol, GPP 5-OH或8-OH Mg2 + >Ni2 + >Co2 + >Mn2 + >Zn2 + >Ca2 + [47] CpPT3 Umbelliferone GPP C-8位 Mg2 + [47] 小苦橙Citrus micrantha Wester CmiPT1a / b Bergaptol和Xanthotoxol GPP 5-OH或8-OH Mg2 + [47] 明日叶Angelica keiskei (Miquel) Koidz. AkPT1 Bergaptol和Xanthotoxol DMAPP 5-OH或8-OH Mg2 + >Mn2 + >Ca2 + [47] 大豆Glycine max (L.) Merr. GmC4DT Coumestrol DMAPP C-4位 Mg2 + >Mn2 + [29] 九里香Murraya exotica L. MePT1 Umbelliferone GPP C-8位、C-6位和7-OH Mg2 + [48] 植物中还存在大量的O-异戊烯基化合物,直到2021年才从芸香科的葡萄柚(Citrus paradisi Macf.)中鉴定出第一个O-异戊烯基转移酶CpPT1,该酶可以催化GPP转移到香豆素的5-OH或8-OH上,形成O-异戊烯基香豆素(附图2:C)。从小苦橙(Citrus micrantha Wester)中得到两个与CpPT1相似度为98%的基因:CmiPT1a和CmiPT1b,可以催化GPP与Bergaptol和Xanthotoxol反应。此外,还从伞形科的明日叶(Angelica keiskei (Miquel) Koidz.)中鉴定出一个O-异戊烯基转移酶AkPT1,该酶可以催化DMAPP与Bergaptol和Xanthotoxol反应[47]。
Li等[48]在芸香科植物九里香(Murraya exotica L.)中得到两个新的PTs:MePT1催化GPP转移到伞形酮的骨架上,同时生成3种化合物:8/6-C-geranylumbelliferone和少量的7-O-geranylumbelliferone;MePT2催化DMAPP转移到喹诺酮类生物碱N-methylquinolone的C-3位生成C-异戊烯基化合物。这是首次报道植物PT同时催化产生C-和O-异戊烯基化合物,并且利用喹诺酮类生物碱作为异戊烯基受体。
呋喃香豆素和吡喃香豆素在植物中分布广泛,已经在部分植物发现UDT催化伞形酮的异戊烯基化反应是角型和线型呋喃香豆素形成的第一步。香豆素O-异戊烯基转移酶基因的发现,为更多的O-异戊烯基转移酶的鉴定工作奠定基础。
2.3 其它次生代谢物合成相关的异戊烯基转移酶
大麻科中的啤酒花(Humulus lupulus L.)雌花序是生产啤酒的基本原料,间苯三酚衍生物(包括α-苦味酸(律草酮Humulone)、β-苦味酸(蛇麻酮Lupulone)和黄腐酚(Xanthohumol,XN))为啤酒风味物质。Tsurumaru等[39]从啤酒花鉴定出的HlPT-1,可以催化DMAPP与Phlorisovalerophenone(PIVP)、Phlorisobutyrophenone(PIBP)和 Phlormethylbutanophenone(PMBP)反应。HlPT-1催化一个异戊烯基基团转移到PIVP上,这是苦味酸生物合成的第步异戊烯基化反应。HlPT-1还可催化DMAPP与柚皮素查尔酮(Naringenin chalcone)反应,生成Desmethylxanthohumol,可进一步合成黄腐酚。Li等[49]从啤酒花栽培品“Nugget”中克隆得到两个芳香族异戊烯基转移酶基因,其中一个基因与HlPT-1的一致性为98.5%,命名为HlPT1-like(HlPT1L),另一个基因命名为HlPT2。在包含上游基因的优化的酵母系统中,HlPT1L和HlPT2共表达可高效地催化苦味酸合成途径的异戊烯基化反应,并揭示出在β-苦味酸生物合成中,HlPT1L催化第1步异戊烯基化反应,而HlPT2负责第2和第3步异戊烯基化反应。研究表明,HlPT1L与HlPT2能够相互作用,形成异源二聚体或多聚体,这是首次在植物中发现了芳香族异戊烯基转移酶形成复合物,催化多步连续的异戊烯基化反应。
氧杂蒽酮(Xanthone)在植物中具有抗病原微生物和防御食草动物的作用。Fiesel等[50]从冬绿金丝桃(Hypericum calycinum L.)中鉴定出的氧杂蒽酮异戊烯基转移酶HcPT,催化DMAPP与1,3,6,7-Tetrahydroxyxanthone(1367THX)反应生成1,3,6,7-Tetrahydroxy-8-prenylxanthone(8PX)。Nagia等[51]从冬绿金丝桃和元宝草(H. sampsonii Hance)中鉴定出4个氧杂蒽酮异戊烯基转移酶:HcPT8px、HcPTpat、HsPT8px和HsPTpat,HcPT8px和HsPT8px主要可以催化DMAPP与1367THX反应生成8PX,HsPT8px进一步可以催化DMAPP与8PX反应生成少量的Patulone,而HcPTpat和HsPTpat可催化两个DMAPP直接与1367THX反应生成Patulone,也可催化8PX生成Patulone(附图2:D)。
二苯乙烯类化合物(Stilbenoids)是植物抗毒素中最常见的一种,也具有心脏保护、抗炎以及神经保护等广泛的活性[52]。Yang等[53]从豆科植物落花生(Arachis hypogaea L.)中发现了AhR4DT-1和AhR3'DT-1 / 2 / 3 / 4,AhR4DT-1可催化DMAPP与白藜芦醇(Resveratrol)、白皮杉醇(Piceatannol)和赤松素(Pinosylvin)的C-4位反应(附图2:E),还可以催化氧化白藜芦醇(Oxyresveratrol),但催化位点不确定。AhR3′DT-1催化白藜芦醇C-3′位异戊烯基化,以及白皮杉醇和氧化白藜芦醇(催化位点不确定),但不能催化赤松素的异戊烯基化。Zhong等[54]从桑中鉴定得到MaOGT主要催化GPP转移到氧化白藜芦醇的C-4位,对白藜芦醇也有微弱的催化活性。此外,MaOGT还可以接受DMAPP、FPP、IPP和GGPP作为异戊烯基供体,催化氧化白藜芦醇生成少量的产物。
Munakata等[55]从茵陈蒿(Artemisia capillaris Thunb.)里发现一个参与苯丙烷生物合成的异戊烯基转移酶AcPT1,该酶可催化DMAPP与对香豆酸(p-Coumaric acid)反应,生成两种产物Drupanin和Artepillin C。此外,实验证明该酶可接受Drupanin作为底物,生成Artepillin C(附图2:F),说明AcPT1逐步转移两个异戊烯基(DMAPP)到对香豆酸羟基的邻位,Drupanin是一种中间产物。
Saeki等[56]从兴安杜鹃(Rhododendron dauricum L.)发现的RdPT1,特异识别Orsellinic acid(2,4-Dihydroxy-6-methylbenzoic acid)作为底物,而对异戊烯基供体的特异性较低,可以高效的催化FPP与底物反应生成Grifolic acid,还接受GPP和GGPP以中等效率合成Grifolic acid类似物。Luo等[57]从大麻(Cannabis sativa L.)中发现的CsPT4可以催化Olivetolic acid(2,4-Dihydroxy-6-pentylbenzoic acid)与GPP反应生成大麻酚酸Cannabigerolic acid(CBGA)。
3. 植物次生与初生代谢物合成PTs的系统关系分析
根据目前已鉴定的植物中UbiA膜结合型芳香族异戊烯基转移酶构建了系统发育树(图3)。系统进化分析结果表明,参与植物初生代谢物生物合成的异戊烯基转移酶(PMPTs)可以根据底物类型(对羟基苯甲酸、脱植基叶绿素、亚铁血红素B、1,4-二羟基-2-萘甲酸和尿黑酸)分为5个大组,其中以尿黑酸为底物的HGPT家族又可分为3个亚组,分别参与生育三烯酚、生育酚和质体醌的生物合成。不同植物类群的PMPTs根据其功能(催化底物类型)分别聚在一起。
其中有两个组(分别以对羟基苯甲酸和尿黑酸为底物)发生了产生次生代谢物基因的扩张。第1组,以对羟基苯甲酸为底物的PPTs组,发现5个参与植物次生代谢物紫草素合成的酶(LePGT-1、LePGT-2、AePGT、AePGT4和AePGT6),因此推测其从参与泛醌生物合成的PPTs进化而来。第2组:以尿黑酸为底物的HGPT组,产生了多个类型的PHPTs。这些PHPT并没有按照次生代谢物的底物类型聚在一起,如所有已发现的FPTs,分散在4个不同的小分支中(豆科、小檗科、桑科和大麻科),表现出不同的植物科属独立发生,同科的PHPT聚为一支,每个分支中可能包括多个类型的多酚化合物。如桑科中的香豆素异戊烯基转移酶(FcPT1)和类黄酮异戊烯基转移酶(MaIDT和CtIDT)聚在一起,在分类上与桑科近缘的大麻科中的类黄酮异戊烯基转移酶(CsPT3和CsPT8)和间苯三酚异戊烯基转移酶(HlPT1L和HlPT2)聚在一起,而这两支与质体醌合成相关的VTE2-1亲缘关系较近,因此推测是从质体醌合成相关基因进化而来。豆科的类黄酮异戊烯基转移酶是迄今发现最多的一类,和从豆科中发现的二苯乙烯类异戊烯基转移酶聚为一支,芸香科和伞形科也是同一植物科组成了独立的枝系,包括C-PTs和O-PTs。小檗科的类黄酮异戊烯基转移酶聚为一支,这几个分支与生育酚和生育三烯酚合成相关的PT亲缘关系较近,推测各自独立起源于这一簇。
与异戊烯基连接的多酚类化合物,从结构类型可以分为类黄酮、香豆素、间苯三酚和二苯乙烯类等,以及未来可能发现的其他酚类成分等,除了紫草素,大多从尿黑酸异戊烯基转移酶家族进化而来,同一科的多酚异戊烯基转移酶可能有一致的起源,进而演化出不同的底物选择性。
4. 展望
本文总结了87个植物UbiA膜结合型芳香族异戊烯基转移酶的底物类型和催化特点,包括30个PMPTs和57个PHPTs。PMPTs有非常严格的底物选择性,PHPTs也表现出对底物类型的偏好性,一种PT一般只能催化一种类型的底物,少数可以催化多种类型底物,但对某一种类型的底物催化活性相对较高;PHPTs还表现出对底物催化位点的专一性,邻位有酚羟基的位点更容易发生C-异戊烯基化,O-异戊烯基转移酶报道较少,但也表现出对催化位点的选择性。就异戊烯基供体而言,PMPTs一般可接受C10~C45的中长链异戊烯基,而PHPTs大部分只能接受DMAPP(C5)作为供体,少数可同时接受GPP(C10)作为供体,还有一些只接受GPP作为供体,目前只发现桑中的MaOGT可以接受DMAPP、GPP、FPP(C15)、IPP、GGPP(C20)作为异戊烯基供体,兴安杜鹃中发现的RdPT1可以接受GPP、FPP和GGPP作为供体。相比于植物体内丰富多样的异戊烯基化合物而言,目前报道发现的异戊烯基转移酶基因仍然很少。
许多植物的异戊烯基芳香族化合物在抗炎、抗菌、抗肿瘤、抗氧化等方面具有显著的药理活性。芳香族化合物的异戊烯基化,显著增加了其药理活性和生物利用度。然而,该类化合物在植物中分布有限,且含量较低,通过化学方法合成异戊烯基化合物具有许多局限性,例如修饰位置、数量和立体选择性等。而酵母细胞工厂在合成异戊烯基化合物方面具有潜力,酵母底盘可以提供异戊烯基供体,如DMAPP,通过将特定的异戊烯基转移酶基因转入酵母细胞,利用重组酶对特定的芳香族底物进行定向异戊烯基化[49, 58]。Levisson等[59]将苦参类黄酮异戊烯基转移酶SfFPT引入酿酒酵母菌株PATW066,实现了从头合成8-异戊烯基柚皮素。Wang等[41]报道了使用酿酒酵母菌株CEN.PK2-1C作为细胞工厂,通过修饰12个原生酵母基因,引入11个外源基因(包括淫羊藿类黄酮异戊烯基转移酶EsPT2),构建了能高效生产8-异戊烯基山奈酚的酵母菌株。进一步将GmOMT2引入该酵母菌株的线粒体中,或将该酵母菌与表达GmOMT2的大肠杆菌共培养,产生了具有重要药用价值的淫羊藿素。Luo等[57]在酿酒酵母设计了内源的MVA途径,合成大量的GPP,将橄榄酸(Olivetol acid, OA)合成途径相关的酶以及香叶基转移酶(CsPT4)引入酿酒酵母,构建了大麻酚酸(Cannabigerolic acid,CBGA)、Δ9四氢大麻酚酸(Δ9-Tetrahydrocannabinolic acid,THCA)和大麻二酚酸(Cannabidiolic acid,CBDA)等大麻酚衍生物的全生物合成。然而,PTs参与合成异戊烯基芳香族化合物具有许多挑战:酵母内源的MVA途径定位在内质网或细胞质,而质体定位的PHPTs在没有质体细胞器的酵母中定位是未知的,在化合物合成过程中,酶发挥作用时,对底物和供体的利用率低,这导致异戊烯基化合物的产率低,限制了它们在代谢工程中的应用。
高通量多组学技术的发展,加速了植物功能基因的鉴定,而从目前已报道的PHPTs挖掘策略来看,仍然主要使用传统方法:早期的表达序列标签法(Expressed sequence tag,EST)和同源克隆,这两种方法经常会漏选或筛选到冗余序列,且不能直接获得全长。最近有少量PHPTs基因的发掘是基于基因组或全长转录组的同源搜索,例如通过拟南芥AtVTE2-1序列搜索大豆基因组获得的候选基因,包括GmG2DT、GmC4DT和GmIDT1等[29];通过甘草(Glycyrrhiza uralensis Fisch.)中的GuA6DT序列搜索大麻转录组获得候选基因,如CsPT3[38]。随着生物信息学技术和植物多组学技术的发展,通过基因组学和转录组学联合分析,用基因保守结构域筛选基因家族,并进行系统发育、表达模式、保守基序分析等,可以更全面地筛选候选基因并进行克隆。通过转录组学与代谢组学联合分析,发现不同处理下异戊烯基化合物的含量差异,挖掘这类化合物生物合成的候选基因。更多芳香族异戊烯基转移酶被克隆并鉴定,有助于我们更好地了解该类酶的进化关系及催化机制,解析化合物的生物合成途径,进一步为生物代谢工程和优良品种的培育奠定基础。
1 1,2)如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。 -
表 1 36份猕猴桃种质果实采收时的成熟度
Table 1 Fruit maturity at harvest of 36 Actinidia accessions
种类名称
Class name种质名称
Accession name单果重
Fresh weight / g硬度
Firmness / N可溶性固形物
Soluble solids content / %干物质
Dry matter / %美味 ‘金美’ 63.13 ± 0.94 78.07 ± 1.54 7.52 ± 0.30 23.48 ± 0.22 美味 ‘东玫’ 52.79 ± 2.02 84.92 ± 3.52 7.55 ± 0.35 21.19 ± 0.44 美味 ‘金魁’ 99.98 ± 3.90 88.94 ± 3.56 7.52 ± 0.21 19.80 ± 0.38 美味 ‘米良1号’ 104.65 ± 0.83 65.98 ± 2.26 7.88 ± 0.32 19.02 ± 0.26 美味 ‘徐香’ 78.15 ± 3.54 89.93 ± 3.05 7.61 ± 0.22 18.97 ± 0.27 美味 ‘楚红’ 50.10 ± 1.43 49.67 ± 3.08 7.04 ± 0.36 18.77 ± 0.24 美味 ‘海沃德’ 115.03 ± 1.23 67.91 ± 1.75 7.18 ± 0.24 16.56 ± 0.23 美味平均值 80.55 ± 1.98 75.06 ± 2.68 7.47 ± 0.29 19.68 ± 0.29 中华 ‘华优’ 84.01 ± 1.98 53.34 ± 1.64 9.78 ± 0.55 20.95 ± 0.31 中华 翠玉实生12617 74.83 ± 1.91 59.03 ± 2.42 10.74 ± 0.42 20.46 ± 0.24 中华 中华杂交CD611 61.49 ± 1.21 61.39 ± 1.72 9.15 ± 0.29 19.09 ± 0.20 中华 ‘翠玉’ 69.32 ± 3.28 62.77 ± 2.21 9.91 ± 0.45 18.72 ± 0.43 中华 ‘武植3号’ 82.76 ± 3.61 56.65 ± 3.71 9.24 ± 0.62 18.44 ± 0.31 中华 ‘金早’ 79.51 ± 1.76 56.11 ± 1.94 7.80 ± 0.43 18.38 ± 0.35 中华 中华杂交CD11129 55.53 ± 1.82 62.19 ± 1.99 8.34 ± 0.26 18.34 ± 0.26 中华 ‘金玉’ 107.01 ± 2.67 54.14 ± 1.80 8.01 ± 0.33 18.11 ± 0.27 中华 ‘东红’ 112.28 ± 2.92 53.26 ± 1.66 8.79 ± 0.52 16.81 ± 0.37 中华 ‘金霞’ 103.08 ± 0.98 53.87 ± 1.79 8.55 ± 0.35 16.47 ± 0.18 中华 ‘金桃’ 148.26 ± 7.88 55.61 ± 1.65 9.12 ± 0.45 16.29 ± 0.27 中华 ‘金农’ 95.09 ± 3.84 45.50 ± 3.34 8.32 ± 0.37 15.22 ± 0.24 中华 ‘金丰’ 109.61 ± 2.77 60.97 ± 2.14 8.45 ± 0.15 15.06 ± 0.18 中华 ‘丰悦’ 111.04 ± 2.04 46.84 ± 2.96 7.53 ± 0.37 14.74 ± 0.25 ‘金艳’ × 中华 ‘金圆’ 116.14 ± 2.39 60.95 ± 1.34 9.36 ± 0.39 16.71 ± 0.19 ‘金艳’ × 中华 ‘金梅’ 102.27 ± 2.18 59.26 ± 1.63 8.27 ± 0.19 16.68 ± 0.24 中华平均值 94.51 ± 2.70 56.37 ± 2.12 8.84 ± 0.38 17.53 ± 0.27 山梨 × 中华 ‘中科绿猕7号’ 43.65 ± 0.51 66.98 ± 2.45 8.07 ± 0.22 17.86 ± 0.32 山梨 × 中华 山梨 × 中华F1-AC17 43.93 ± 0.53 47.00 ± 3.05 9.82 ± 0.26 17.73 ± 0.13 山梨 × 中华 ‘中科绿猕8号’ 41.97 ± 0.73 58.52 ± 1.66 9.00 ± 0.24 17.51 ± 0.15 山梨 × 中华 山梨 × 中华F1-AC18 38.31 ± 0.88 59.79 ± 3.10 11.50 ± 0.22 17.00 ± 0.15 山梨 × 中华 山梨 × 中华F1-AC16 45.45 ± 0.79 46.83 ± 1.47 9.38 ± 0.21 16.69 ± 0.22 山梨 × 中华 ‘中科绿猕9号’ 48.99 ± 0.91 33.80 ± 3.04 11.78 ± 0.21 16.41 ± 0.13 山梨 × 中华 山梨 × 中华F1-AC15 45.61 ± 0.94 57.16 ± 2.69 9.66 ± 0.16 16.23 ± 0.13 山梨 × 中华 ‘中科绿猕6号’ 44.66 ± 0.58 46.75 ± 1.57 10.25 ± 0.19 15.87 ± 0.20 山梨 × 中华 ‘中科绿猕5号’ 41.92 ± 1.11 47.73 ± 1.88 10.05 ± 0.15 15.35 ± 0.19 山梨 × 中华平均值 43.83 ± 0.78 51.62 ± 2.32 9.95 ± 0.21 16.74 ± 0.18 中华 × ‘超红’ ‘中科绿猕12号’ 36.46 ± 0.63 67.20 ± 1.55 8.31 ± 0.16 18.31 ± 0.17 中华 × ‘超红’ ‘中科绿猕10号’ 28.34 ± 0.86 56.06 ± 2.78 9.75 ± 0.30 17.31 ± 0.12 中华 × ‘超红’ ‘中科绿猕11号’ 33.44 ± 0.84 35.76 ± 2.01 10.03 ± 0.16 15.51 ± 0.15 中华 × ‘超红’ 毛花b754 32.70 ± 0.77 45.94 ± 2.78 7.99 ± 0.15 12.92 ± 0.21 中华 × ‘超红’平均值 32.74 ± 0.78 51.24 ± 2.28 9.02 ± 0.19 16.01 ± 0.16 总体 平均值 72.26 58.25 8.87 17.58 最小值 28.34 33.80 7.04 12.92 最大值 148.26 89.93 11.78 23.48 标准差 31.51 12.71 1.19 2.06 变异系数 / % 43.61 21.81 13.39 11.72 表 2 36份猕猴桃种质的软熟果实感官评价
Table 2 Sensory evaluation of ripe fruit of 36 Actinidia accessions
种类名称
Class name种质名称
Accession name整体喜好度
Overall liking风味喜好度
Flavor liking风味强烈程度
Flavor intensity甜度
Sweetness酸度
Acidity接受度
Acceptance美味 ‘徐香’ 6.05 ± 0.25 6.00 ± 0.21 5.75 ± 0.19 5.90 ± 0.22 4.55 ± 0.33 85 美味 ‘金美’ 5.95 ± 0.26 6.11 ± 0.25 6.00 ± 0.22 5.37 ± 0.21 4.42 ± 0.29 73.68 美味 ‘东玫’ 5.85 ± 0.26 5.95 ± 0.32 5.85 ± 0.22 5.70 ± 0.22 4.85 ± 0.3 60 美味 ‘金魁’ 5.32 ± 0.26 5.26 ± 0.28 6.00 ± 0.24 5.12 ± 0.33 5.65 ± 0.36 58.82 美味 ‘米良1号’ 5.06 ± 0.22 5.22 ± 0.24 5.22 ± 0.22 4.83 ± 0.17 5.17 ± 0.25 44.44 美味 ‘楚红’ 4.74 ± 0.38 4.88 ± 0.39 5.03 ± 0.38 4.76 ± 0.48 5.00 ± 0.33 35.29 美味 ‘海沃德’ 4.20 ± 0.40 4.63 ± 0.48 5.47 ± 0.43 4.40 ± 0.36 5.97 ± 0.47 13.33 美味平均值 5.31 ± 0.29 5.44 ± 0.31 5.62 ± 0.27 5.15 ± 0.28 5.09 ± 0.33 52.94 中华 ‘华优’ 7.19 ± 0.37 7.31 ± 0.28 6.69 ± 0.31 7.06 ± 0.3 3.50 ± 0.42 87.5 中华 ‘东红’ 6.90 ± 0.31 6.65 ± 0.33 5.90 ± 0.24 6.20 ± 0.3 3.55 ± 0.45 70 中华 翠玉实生12617 6.00 ± 0.21 5.50 ± 0.17 6.05 ± 0.28 5.63 ± 0.25 5.08 ± 0.32 68.42 中华 ‘金桃’ 5.63 ± 0.31 5.70 ± 0.31 4.60 ± 0.32 5.15 ± 0.22 4.80 ± 0.32 65 中华 ‘金早’ 5.56 ± 0.36 5.50 ± 0.48 4.81 ± 0.4 4.97 ± 0.36 4.19 ± 0.42 81.25 中华 ‘金霞’ 5.43 ± 0.26 5.53 ± 0.29 5.60 ± 0.35 4.78 ± 0.25 5.70 ± 0.28 70 中华 ‘翠玉’ 5.06 ± 0.26 4.82 ± 0.33 5.06 ± 0.3 4.65 ± 0.3 4.06 ± 0.37 29.41 中华 ‘金农’ 4.83 ± 0.44 4.60 ± 0.52 5.37 ± 0.44 4.77 ± 0.41 5.60 ± 0.36 46.67 中华 ‘金玉’ 4.75 ± 0.4 4.95 ± 0.34 5.40 ± 0.26 5.55 ± 0.26 4.50 ± 0.34 40 中华 中华杂交CD611 4.70 ± 0.18 4.75 ± 0.19 5.30 ± 0.15 4.20 ± 0.37 6.30 ± 0.4 20 中华 ‘武植3号’ 4.38 ± 0.33 3.92 ± 0.31 5.54 ± 0.31 3.38 ± 0.27 6.69 ± 0.35 7.69 中华 中华杂交CD11129 4.26 ± 0.3 4.47 ± 0.16 5.05 ± 0.28 3.58 ± 0.33 6.53 ± 0.34 5.26 中华 ‘丰悦’ 3.63 ± 0.31 3.69 ± 0.36 3.06 ± 0.35 3.31 ± 0.38 4.50 ± 0.29 12.5 中华 ‘金丰’ 1.80 ± 0.29 2.50 ± 0.27 5.10 ± 0.86 1.90 ± 0.31 6.80 ± 0.66 0 ‘金艳’ × 中华 ‘金圆’ 5.47 ± 0.39 5.21 ± 0.37 5.84 ± 0.36 5.11 ± 0.37 5.63 ± 0.35 47 ‘金艳’ × 中华 ‘金梅’ 5.17 ± 0.29 5.33 ± 0.26 5.56 ± 0.23 5.17 ± 0.22 5.56 ± 0.29 38.89 中华平均值 5.05 ± 0.31 5.03 ± 0.31 5.31 ± 0.34 4.71 ± 0.31 5.19 ± 0.37 43.1 山梨 × 中华 山梨 × 中华F1-AC16 6.65 ± 0.24 6.50 ± 0.29 5.15 ± 0.24 6.08 ± 0.3 4.25 ± 0.2 65 山梨 × 中华 ‘中科绿猕9号’ 6.55 ± 0.29 6.15 ± 0.32 5.55 ± 0.21 5.80 ± 0.27 4.25 ± 0.3 80 山梨 × 中华 ‘中科绿猕7号’ 6.52 ± 0.25 6.38 ± 0.28 5.95 ± 0.31 5.86 ± 0.28 4.76 ± 0.45 76.19 山梨 × 中华 山梨 × 中华F1-AC15 6.14 ± 0.27 6.19 ± 0.34 7.00 ± 0.32 5.90 ± 0.35 4.71 ± 0.4 61.91 山梨 × 中华 ‘中科绿猕6号’ 5.81 ± 0.31 5.62 ± 0.35 5.45 ± 0.32 5.48 ± 0.34 3.71 ± 0.35 61.91 山梨 × 中华 山梨 × 中华F1-AC17 5.80 ± 0.26 5.65 ± 0.33 4.95 ± 0.3 5.30 ± 0.38 4.55 ± 0.21 60 山梨 × 中华 山梨 × 中华F1-AC18 5.70 ± 0.35 5.60 ± 0.33 5.80 ± 0.32 5.60 ± 0.28 4.65 ± 0.29 65 山梨 × 中华 ‘中科绿猕8号’ 5.19 ± 0.27 4.62 ± 0.28 4.67 ± 0.28 4.57 ± 0.3 4.05 ± 0.37 38.1 山梨 × 中华 ‘中科绿猕5号’ 4.95 ± 0.36 4.89 ± 0.39 5.11 ± 0.37 4.58 ± 0.4 4.42 ± 0.38 42.11 山梨 × 中华平均值 5.92 ± 0.29 5.73 ± 0.32 5.51 ± 0.3 5.46 ± 0.32 4.37 ± 0.33 61.14 中华 × ‘超红’ ‘中科绿猕12号’ 5.88 ± 0.18 5.81 ± 0.28 5.06 ± 0.41 5.06 ± 0.41 4.00 ± 0.68 68.75 中华 × ‘超红’ ‘中科绿猕11号’ 5.40 ± 0.28 4.93 ± 0.29 4.20 ± 0.32 4.40 ± 0.3 3.40 ± 0.47 55 中华 × ‘超红’ ‘中科绿猕10号’ 4.60 ± 0.35 4.15 ± 0.39 3.40 ± 0.43 3.85 ± 0.32 4.10 ± 0.4 30 中华 × ‘超红’ 毛花b754 3.73 ± 0.38 3.53 ± 0.42 3.37 ± 0.49 3.57 ± 0.35 3.67 ± 0.43 13.33 中华 × ‘超红’平均值 4.90 ± 0.3 4.61 ± 0.35 4.01 ± 0.41 4.22 ± 0.35 3.79 ± 0.5 41.77 总体 平均值 5.30 5.24 5.28 4.93 4.81 49.37 最小值 1.80 2.50 3.06 1.90 3.40 0.00 最大值 7.19 7.31 7.00 7.06 6.80 87.50 标准差 1.03 0.96 0.82 0.99 0.92 24.67 变异系数 / % 19.48 18.35 15.59 20.07 19.06 49.96 -
[1] 黄宏文. 猕猴桃属分类资源驯化栽培[M]. 北京: 科学出版社, 2013: 2. [2] 钟彩虹,黄文俊,李大卫,张琼,李黎. 世界猕猴桃产业发展及鲜果贸易动态分析[J]. 中国果树,2021(7):101−108. Zhong CH,Huang WJ,Li DW,Zhang Q,Li L. Dynamic analysis of global kiwifruit industry development and fresh fruit trade[J]. China Fruits,2021 (7):101−108.
[3] 方金豹,钟彩虹. 新中国果树科学研究70年——猕猴桃[J]. 果树学报,2019,36(10):1352−1359. Fang JB,Zhong CH. Fruit scientific research in New China in the past 70 years:kiwifruit[J]. Journal of Fruit Science,2019,36 (10):1352−1359.
[4] Zhong HC,Huang WJ,Wang ZP,Li L,Li DW,et al. The breeding progress and development status of the kiwifruit industry in China[J]. Acta Hortic,2022,1332:445−454.
[5] Huang HW,Wang Y,Zhang ZH,Jiang ZW,Wang SM. Actinidia germplasm resources and kiwifruit industry in China[J]. HortScience,2004,39 (6):1165−1172. doi: 10.21273/HORTSCI.39.6.1165
[6] 黄宏文,龚俊杰,王圣梅,何子灿,张忠慧,李建强. 猕猴桃属(Actinidia)植物的遗传多样性[J]. 生物多样性,2000,8(1):1−12. Huang HW,Gong JJ,Wang SM,He ZC,Zhang ZH,Li JQ. Genetic diversity in the genus Actinidia[J]. Chinese Biodiversity,2000,8 (1):1−12.
[7] Zhang HX,Zhao QY,Lan T,Geng TH,Gao CX,et al. Comparative analysis of physicochemical characteristics,nutritional and functional components and antioxidant capacity of fifteen kiwifruit (Actinidia) cultivars-comparative analysis of fifteen kiwifruit (Actinidia) cultivars[J]. Foods,2020,9 (9):1267. doi: 10.3390/foods9091267
[8] Ma TT,Sun XY,Zhao JM,You YL,Lei YS,et al. Nutrient compositions and antioxidant capacity of kiwifruit (Actinidia) and their relationship with flesh color and commercial value[J]. Food Chem,2017,218:294−304. doi: 10.1016/j.foodchem.2016.09.081
[9] 黄文俊,江昌应,陈美艳,刘小莉,张琦,等. 三个产地猕猴桃品种‘金梅’在低温贮藏及货架期内的采后生理和品质变化[J]. 植物科学学报,2020,38(5):687−695. Huang WJ,Jiang CY,Chen MY,Liu XL,Zhang Q,et al. Changes in postharvest physiology and fruit quality of Actinidia chinensis Planch. ‘Jinmei’ from three different production regions during cool storage and shelf life[J]. Plant Science Journal,2020,38 (5):687−695.
[10] 刘璐,屈振江,张勇,李艳莉. 陕西猕猴桃果品气候品质认证模型构建[J]. 陕西气象,2017(4):21−25. [11] 肖涛,程均欢,刘涛,肖丽丽,王华玲,等. 不同授粉方式对猕猴桃果实性状的影响[J]. 中国南方果树,2022,51(3):122−125. [12] 易淑瑶,刘青,贾东峰,李亦淇,黄春辉,等. 不同结果母枝粗度对“东红”猕猴桃果实品质的影响[J]. 中国南方果树,2020,49(4):122−126. [13] Chai JX,Wang YT,Liu YF,Gu ZM,Liu ZD. High O2/N2 controlled atmosphere accelerates postharvest ripening of ‘Hayward’ kiwifruit[J]. Sci Hortic,2022,300:111073. doi: 10.1016/j.scienta.2022.111073
[14] 王依,雷靖,陈成,徐明,邴昊阳,雷玉山. 美味猕猴桃新品种‘瑞玉’果实品质综合评价[J]. 西北农林科技大学学报(自然科学版),2018,46(10):101−107. Wang Y,Lei J,Chen C,Xu M,Bing HY,Lei YS. Comprehensive evaluation of fruit quality of a new delicious kiwifruit variety ‘Ruiyu’[J]. Journal of Northwest A& F University (Natural Science Edition)
,2018,46 (10):101−107. [15] 陈美艳,赵婷婷,刘小莉,韩飞,张鹏,钟彩虹. 猕猴桃品种‘金艳’果实品质因子分析与综合评价[J]. 植物科学学报,2021,39(1):85−92. Chen MY,Zhao TT,Liu XL,Han F,Zhang P,Zhong CH. Factor analysis and comprehensive evaluation of fruit quality of ‘Jinyan’ kiwifruit (Actinidia eriantha × Actinidia chinensis)[J]. Plant Science Journal,2021,39 (1):85−92.
[16] 刘磊,李争艳,雷华,高本旺,赵佳,李薇. 30个猕猴桃品种(单株)主要果实品质特征的综合评价[J]. 果树学报,2021,38(4):530−537. Liu L,Li ZY,Lei H,Gao BW,Zhao J,Li W. Comprehensive evaluation of main fruit quality characteristics with 30 kiwifruit cultivars (strains)[J]. Journal of Fruit Science,2021,38 (4):530−537.
[17] 刘科鹏,黄春辉,冷建华,陈葵,严玉平,等. ‘金魁’猕猴桃果实品质的主成分分析与综合评价[J]. 果树学报,2012,29(5):867−871. Liu KP,Huang CH,Leng JH,Chen K,Yan YP,et al. Principal component analysis and comprehensive evaluation of the fruit quality of ‘Jinkui’ kiwifruit[J]. Journal of Fruit Science,2012,29 (5):867−871.
[18] 郭琳琳,庞荣丽,王瑞萍,乔成奎,田发军,等. 猕猴桃营养品质综合评价[J]. 果树学报,2022,39(10):1864−1872. Guo LL,Pang RL,Wang RP,Qiao CK,Tian FJ,et al. Comprehensive trait evaluation for kiwifruit nutritional quality[J]. Journal of Fruit Science,2022,39 (10):1864−1872.
[19] 李跃红,冉茂乾,徐孟怀,陈露,游元丁,等. 不同品种猕猴桃果实品质比较与综合评价[J]. 食品与发酵工业,2020,46(23):162−168. Li YH,Ran MQ,Xu MH,Chen L,You YD,et al. Comparison and comprehensive evaluation of fruit quality of different varieties of kiwifruit[J]. Food and Fermentation Industries,2020,46 (23):162−168.
[20] 赵金梅,高贵田,薛敏,耿鹏飞,孙翔宇,等. 不同品种猕猴桃果实的品质及抗氧化活性[J]. 食品科学,2014,35(9):118−122. Zhao JM,Gao GT,Xue M,Geng PF,Sun XY,et al. Fruit quality and antioxidant activity of different kiwifruit varieties[J]. Food Science,2014,35 (9):118−122.
[21] 陈永安,陈鑫,刘艳飞,杨宏. 基于模糊数学的猕猴桃感官评定分析[J]. 食品工业,2013,34(10):129−133. Chen YA,Chen X,Liu YF,Yang H. Analysis of an improved sensory comprehensive evaluation for kiwifruit based on fuzzy mathematics[J]. The Food Industry,2013,34 (10):129−133.
[22] 吕新刚,王智荣,杨琦,孟官丽. 不同处理对生鲜电商模式下“徐香”猕猴桃常温品质变化的影响[J]. 食品工业科技,2018,39(4):268−273,279. LÜ XG,Wang ZR,Yang Q,Meng GL. Effects of different treatment on quality changes of ‘Xu Xiang’ kiwifruit stored at room temperature under the supply pattern of e-commerce[J]. Science and Technology of Food Industry,2018,39 (4):268−273,279.
[23] 陈璐,廖光联,杨聪,黄春辉,钟敏,等. 基于主成分分析与聚类分析的黄肉猕猴桃品种(系)主要果实性状的综合评价[J]. 江西农业大学学报,2018,40(6):1231−1240. Chen Lu,Liao GL,Yang C,Hung CH,Zhong M,et al. Comprehensive evaluation of main fruit characters of yellow flesh kiwifruit cultivars (strains) based on principal component analysis and cluster analysis[J]. Acta Agriculturae Universitatis Jiangxiensis,2018,40 (6):1231−1240.
[24] 赵治兵,谢国芳,曹森,马立志. 基于主成分分析评价不同基地“贵长”猕猴桃品质特性[J]. 保鲜与加工,2019,19(5):144−148. Zhao ZB,Xie GF,Cao S,Ma LZ. Evaluation of quality characteristics of ‘Guichang’ kiwifruit from different producing regions based on principal component analysis[J]. Storage and Process,2019,19 (5):144−148.
[25] 韩飞,陈美艳,李昆同,黄文俊,闫春林,等. 不同产地‘金圆’猕猴桃低温贮藏下的生理指标及贮藏性变化[J]. 植物科学学报,2018,36(3):381−392. Han F,Chen MY,Li KT,Huang WJ,Yan CL,et al. Changes in physiological indices and storage properties of ‘Jinyuan’ kiwifruit from different orchards under low temperature storage[J]. Plant Science Journal,2018,36 (3):381−392.
[26] 陈双双,贺艳群,徐小彪,陶俊杰,贾东峰,等. 江西省不同产地“金艳”猕猴桃果实品质比较分析[J]. 中国南方果树,2022,51(2):113−116. [27] Burdon J,McLeod D,Lallu N,Gamble J,Petley M,Gunson A. Consumer evaluation of “Hayward” kiwifruit of different at-harvest dry matter contents[J]. Postharvest Biol Technol,2004,34 (3):245−255. doi: 10.1016/j.postharvbio.2004.04.009
[28] Rossiter KL,Young H,Walker SB,Miller M,Dawson DM. The effects of sugars and acids on consumer acceptability of kiwifruit[J]. J Sens Stud,2000,15 (3):241−250. doi: 10.1111/j.1745-459X.2000.tb00269.x
[29] Crisosto G,Hasey JK,Zegbe JA,Crisosto CH. New quality index based on dry matter and acidity proposed for Hayward kiwifruit[J]. Calif Agric,2012,66 (2):70−75. doi: 10.3733/ca.v066n02p70
-
期刊类型引用(0)
其他类型引用(2)
-
其他相关附件
-
PDF格式
申素云附图1-2 点击下载(373KB)
-




 下载:
下载: