Construction of two-hybrid library of yeast and screening of NnWRKY40 interacting proteins in Nelumbo nucifera Gaertn. ‘Baihuajian’
-
摘要:
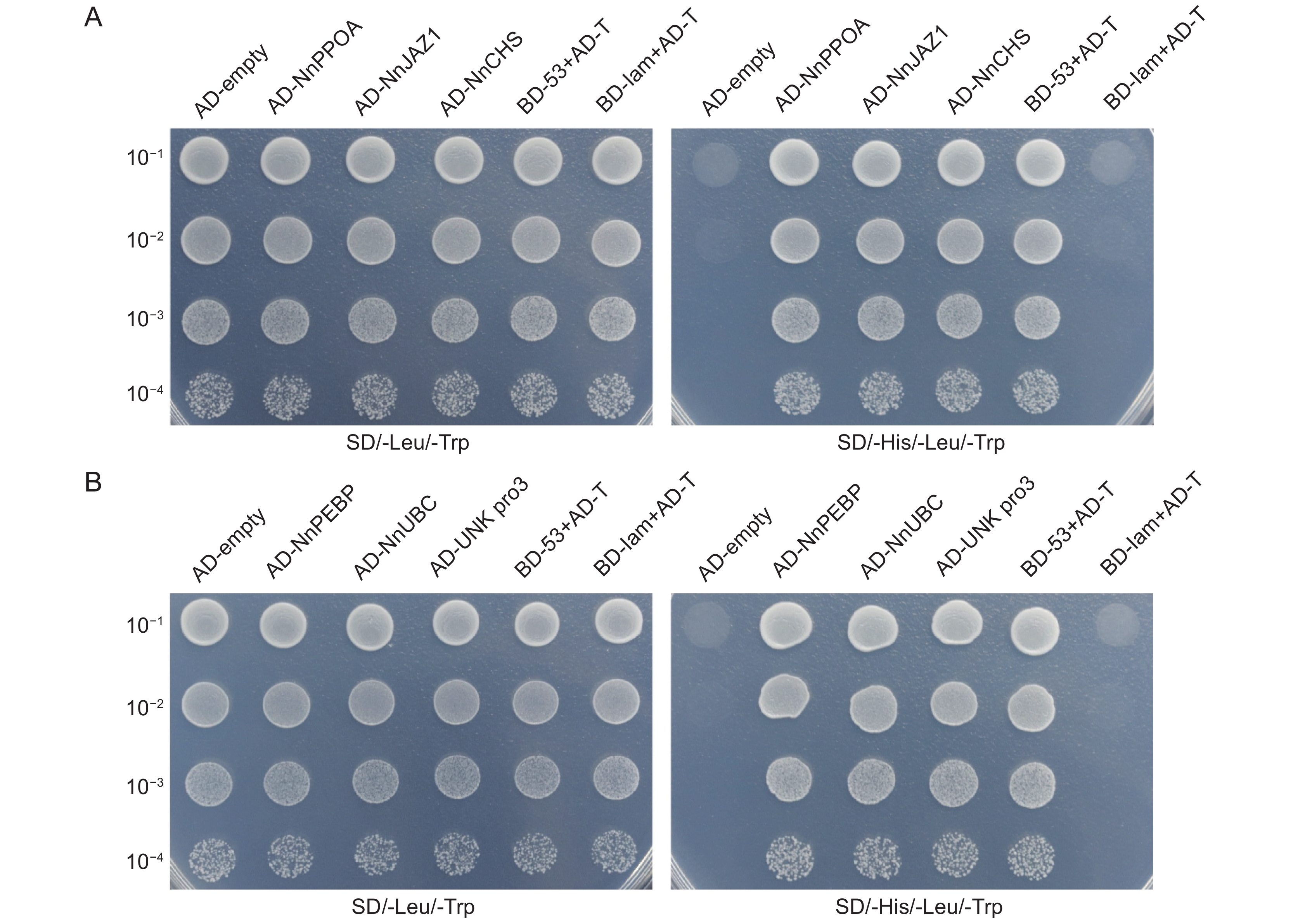
通过构建莲(Nelumbo nucifera Gaertn.)品种 ‘白花建’不同组织的混合cDNA文库,筛选与莲转录因子NnWRKY40互作的蛋白,探究NnWRKY40参与调控次级代谢物生物碱合成的可能机制。结果显示,混合cDNA文库的库容为1.2 × 107 CFU,重组率为100%,插入片段平均长度大于1000 bp。NnWRKY40包含两个同源基因NnWRKY40a和NnWRKY40b,利用NnWRKY40b构建诱饵载体pGBKT7-NnWRKY40b,通过共转化方法,从文库中筛选到27个与NnWRKY40b 互作的蛋白。这些互作蛋白可分为生长发育及抗逆、激素调控和次级代谢、未知蛋白3类。选取6个代表性互作蛋白(NnUBC、NnPEBP、NnPPOA、NnCHS、NnJAZ1和Unknown protein 3)进行一对一验证,发现其中JAZ蛋白与次生代谢物生物碱合成相关,提示NnWRKY40b转录因子可能与茉莉酸(JA)介导的生物碱合成调控密切相关。
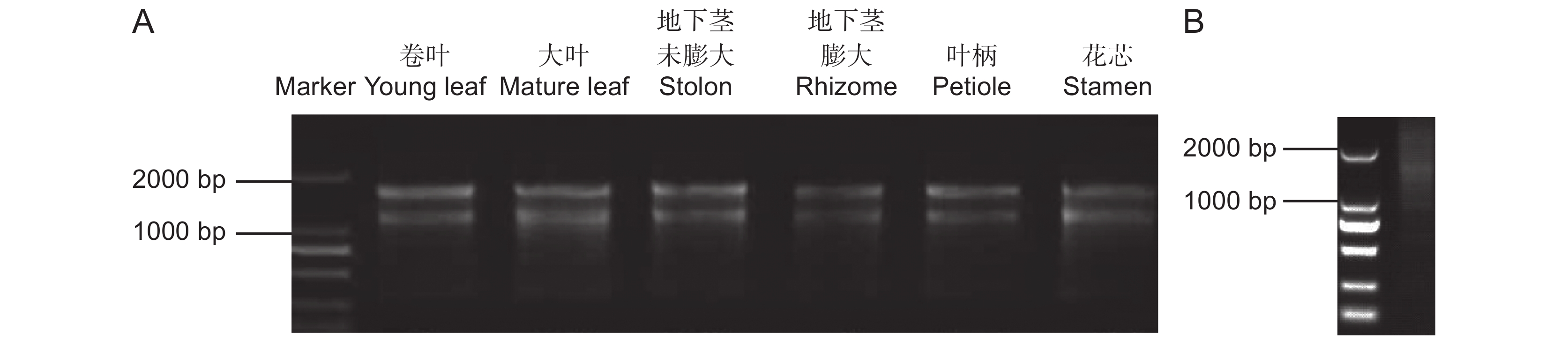
Abstract:To explore the potential mechanism of the NnWRKY40 transcription factor in lotus (Nelumbo nucifera Gaertn.) for regulating the synthesis of secondary metabolite alkaloids, a mixed cDNA library from different lotus tissues was constructed, and the proteins interacting with NnWRKY40 were screened. Total RNA of different tissues was extracted from ‘Baihuajian’, and a mixed cDNA library was established. The library capacity was 1.2 × 107 CFU, recombinant rate was 100%, and average length of the inserted fragments was >1 000 bp. NnWRKY40 contains two homologous genes, NnWRKY40a and NnWRKY40b. As NnWRKY40b is reported to play a leading role in transcriptional activation of alkaloid synthesis genes, we used NnWRKY40b to construct the bait vector PGBKT7-NnWRKY40b. In total, 27 proteins interacting with NnWRKY40b were screened from the library using the co-transformation method. These interacting proteins could be divided into three categories: i.e., growth and development and stress response, hormone regulation and secondary metabolism, and unknown proteins. Six representative proteins, including NnUBC, NnPEBP, NnPPOA, NnCHS, NnJAZ1, and unknown protein 3, were selected for one-to-one verification, among which the JAZ protein was associated with alkaloid synthesis, suggesting that the NnWRKY40b transcription factor may be closely related to jasmonic acid (JA)-mediated regulation of alkaloid synthesis in N. nucifera.
-
Keywords:
- Nelumbo nucifera /
- Yeast two-hybrid /
- NnWRKY40 /
- Protein interaction
-
药材太子参(孩儿参)为石竹科多年生草本植物太子参(Pseudostellaria heterophylla (Miq.)Pax ex Pax et Hoffm.)的干燥块根。它具有益气健脾、生津润肺等多种功效[1-6]。主要分布于我国长江中下游地区,其中江苏、安徽、贵州、福建等省份是太子参主产区。研究发现,不同产地太子参在化学组成和活性成分含量上存在明显差异[7-10]。
太子参皂苷是太子参的主要活性成分之一,具有抗疲劳、耐缺氧、耐低温功效,对视网膜激光损伤具有防护作用[11, 12]。太子参皂苷含量在不同产地有显著差异[13, 14],说明气候条件对药材质量的重要性[15-23]。目前太子参研究主要聚焦于化学成分、药理作用以及加工采收等方面[24, 25],而化学成分和产地气候间的相关性研究却较少[26-28],尤其是缺乏气候因子在不同时间尺度上的响应关系研究。
本研究基于不同产区太子参质量研究影响太子参皂苷的气候响应特征,并在不同时间尺度上剖析气候因子影响的动态变化规律,尝试寻找影响太子参皂苷合成的关键气候因子和气候响应特征,以期为太子参的引种扩种及可持续利用提供科学依据。
1. 材料和方法
1.1 植物材料
太子参样本共14份,分别采自江苏、安徽、贵州以及福建等省,经鉴定均为石竹科植物太子参的块根[29](表1)。
表 1 样本地理信息Table 1. Geographic information of sample省市级
Province and municipality区/县级市
District/county-level city乡镇
Villages and towns编号
Classify and code江苏省镇江市 句容市 袁巷镇 JS-1 江苏省镇江市 句容市 茅山镇 JS-2 江苏省镇江市 句容市 天王镇 JS-3 江苏省镇江市 句容市 天王镇 JS-4 安徽省宣城市 宣州区 黄渡乡 AH-1 安徽省宣城市 宣州区 古泉镇 AH-2 福建省宁德市 柘荣县 富溪镇 FJ 江苏省镇江市 句容市 陈武乡 JS-5 贵州省黔东南州 施秉县 牛大场镇 GZ-1 安徽省宣城市 广德市 东亭乡 AH-3 江苏省常州市 溧阳市 上兴镇 JS-6 江苏省常州市 金坛区 薛埠镇 JS-7 安徽宣城市 宣州区 向阳镇 AH-4 贵州参黔东南州 黄平县 — GZ-2 采用的69个气候数据分别来源于中国气象数据网共享平台和世界气候数据库(http://www. worldclim.org/),为 1970 - 2000年监测数据的平均值,空间分辨率为 30 sec(1 km2);然后是 4 个月均因子,反映气候因子在1 - 12月的动态变化。
1.2 方法
采用紫外-可见分光光度法,在560 nm波长处测定吸光度,以浓度C为横坐标,吸光度A为纵坐标,绘制标准曲线,得回归方程A=0.0208C-0.0042,根据回归方程,求得浓度C,再按:含量(%)=(1.2 × C / 称样量 × 1000) × 100%,计算样品中太子参皂苷的含量。
采用 Excel 2010和 SPSS 25.0软件进行数据分析,运用Prism8.0以及Heml1.0软件绘制图表。通过共线性诊断筛选综合气候因子。采用Analyze-Descriptive Statistics 法标准化处理不同量纲数据,得到标准化结果后进行数据统计分析。聚类分析将数据线性标准化后采用系统聚类法,分析方法采用组间联结,太子参皂苷含量聚类相似度度量采用Pearson 距离法。相关性分析采用 SPSS 25.0软件中双变量Pearson方法进行。不同气候区气候特征采用SPSS 25.0软件描述性分析中的95%置信区间计算。
2. 结果与分析
2.1 太子参皂苷含量地理变异特征
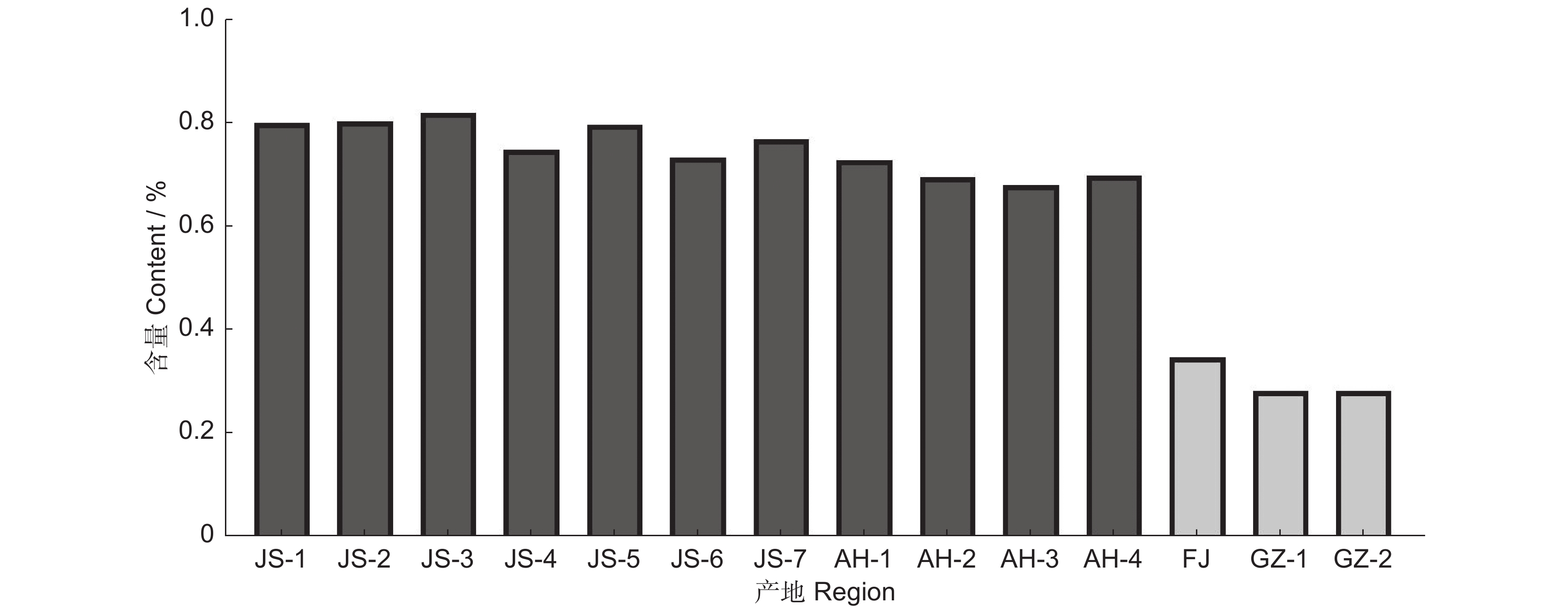
本研究发现,不同产地太子参皂苷含量具有明显的地理变异。江苏、安徽的太子参皂苷含量处于较高水平;而贵州、福建的太子参皂苷含量处于较低水平(图1)。江苏-安徽型太子参皂苷含量平均值为(0.7561 ± 0.0491)%,变幅为0.6840%~0.8239%。其中,江苏句容天王镇朱巷村的太子参皂苷含量最高,为0.8239%;安徽广德县东亭乡的太子参皂苷含量最低,为0.684%。贵州-福建型太子参皂苷含量平均值为(0.3070 ± 0.0377)%,变幅为0.2848%~0.3505%。其中,福建柘荣富溪镇的太子参皂苷含量最高,为0.3505%;贵州黔东南州黄平县的太子参皂苷含量最低,为0.2848%。
2.2 太子参皂苷与气候因子的响应
基于年-季-月3个时间尺度的气候因子分析太子参皂苷含量与气候因子之间的多层次响应关系,以得到气候因子对太子参皂苷累积的动态变化规律以及关键时间窗口。
2.2.1 年均气候因子
依据太子参样本产地的年均气候因子聚类结果(图2):江苏和安徽两地为年均高日照量型(气候型Ⅰ);而贵州和福建两地为低日照量型(气候型Ⅱ)。其中,年均日照量和年均相对湿度是两种气候类型的主要差异因子。气候型Ⅰ的年均日照量明显高于气候型Ⅱ,年均日照量相差约591.45 kJ·m−2·d−1;同时,气候型Ⅱ年均相对湿度稍高于气候型Ⅰ,两种气候类型的年均相对湿度相差约15%。
![]() 图 2 不同产地年均因子热图JS:江苏;AH:安徽;GZ:贵州;FJ:福建。NJS:年降水;NJW:年均温;RZ:年均日照时数;SD:年均相对湿度。下同。Figure 2. Heatmap of annual climate factorsJS: Jiangsu; AH: Anhui; GZ: Guizhou; FJ: Fujian. NJS: Average annual precipitation; NJW: Average annual temperature; RZ: Sunshine duration; SD: Average annual humidity. Same below.
图 2 不同产地年均因子热图JS:江苏;AH:安徽;GZ:贵州;FJ:福建。NJS:年降水;NJW:年均温;RZ:年均日照时数;SD:年均相对湿度。下同。Figure 2. Heatmap of annual climate factorsJS: Jiangsu; AH: Anhui; GZ: Guizhou; FJ: Fujian. NJS: Average annual precipitation; NJW: Average annual temperature; RZ: Sunshine duration; SD: Average annual humidity. Same below.同时,两种气候类型间的其他年均因子也稍有差异。其中,两种气候型的年均降水平均值相差约218.4 mm,而年均温平均值差值约0.2 ℃。
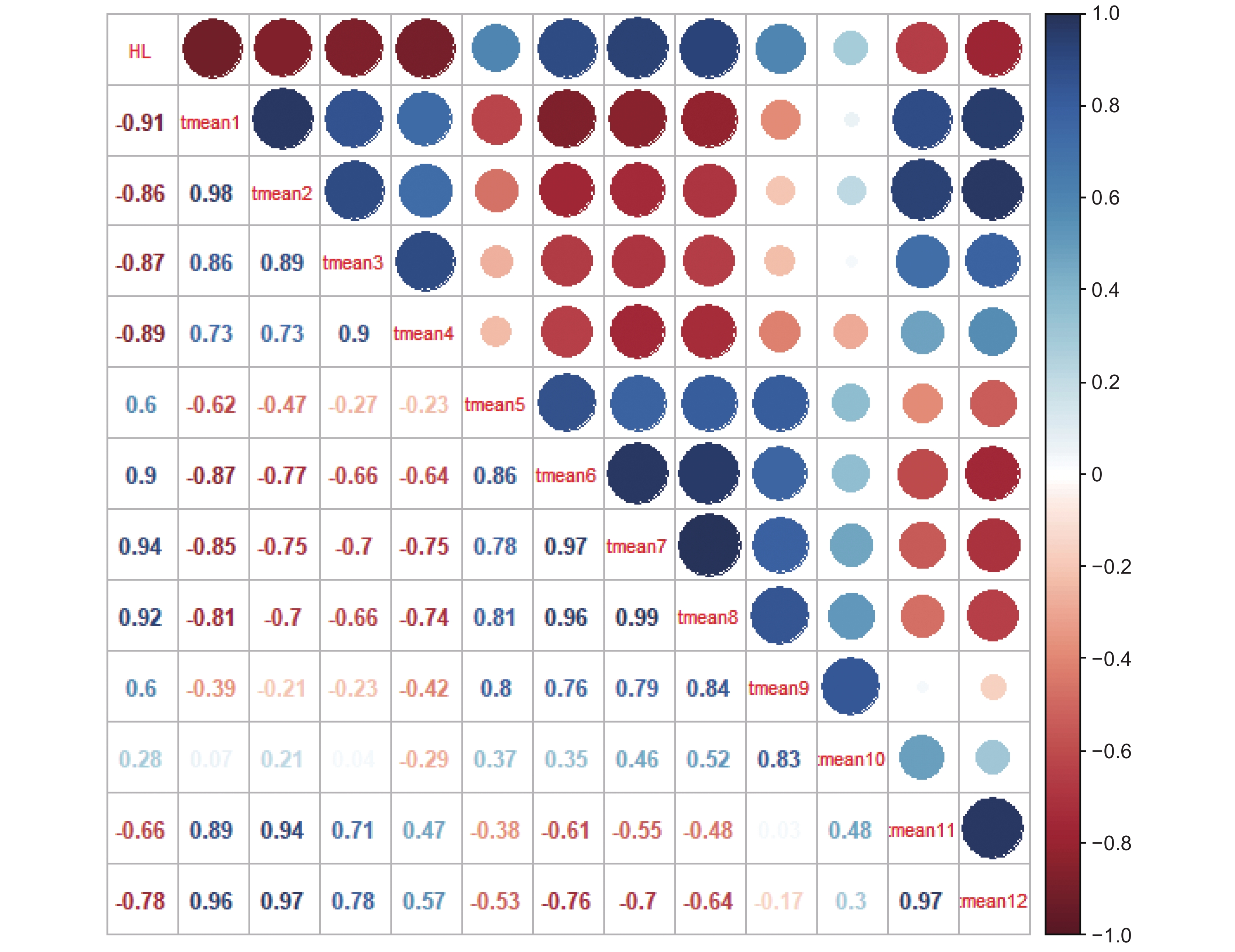
为定量分析年均气候因子与太子参皂苷含量的响应关系,采用Pearson系数法计算各地太子参皂苷含量与年均气候因子间的相关性(图3)。
由图3可知,与太子参皂苷含量有明显相关性的气候因子是年均日照时数、年均相对湿度和年均降水量,而与年均温相关性不显著。其中,太子参皂苷含量与年均日照量呈极显著正相关,说明一定条件下日照量越高,越有利于太子参皂苷的积累,另外,太子参皂苷含量与年均降水和年均相对湿度均呈负相关,说明水分因子量越低,太子参皂苷含量越高,即少雨、低湿可能更适宜太子参皂苷的产生与积累。同时,由相对系数可知,年均相对湿度对太子参皂苷含量的影响程度略大于年均降水。
2.2.2 季度因子
通过共线性诊断保留的11个bio综合气候因子(bio2、bio3、bio5、bio7、bio8、bio9、bio11、bio14、bio15、bio18、bio19),计算太子参皂苷含量和这些气候因子间的相关系数(表2)。
表 2 太子参皂苷含量与季度气候因子间的Pearson系数Table 2. Pearson correlation coefficients between seasonal climatic factors and saponin content气候因子
Climate factor相关系数
Correlation coefficient显著性(双尾)
Sig.气候因子
Climate factor相关系数
Correlation coefficient显著性(双尾)
Sig.bio2 0.423 0.132 bio11 −0.863** 0.000 bio3 −0.923** 0.000 bio14 0.315 0.272 bio5 0.893** 0.000 bio15 −0.775** 0.001 bio7 0.961** 0.000 bio18 −0.475 0.086 bio8 0.853** 0.000 bio19 0.290 0.314 bio9 −0.146 0.619 注:** 表示0.01 级别(双尾)相关性显著。下同。 Note: ** indicates significant differences at P < 0.01 level. Same below. 太子参皂苷含量与6个综合气候因子间具有显著相关性,其中,5个温度因子分别是bio3(昼夜温差与年温差比值)、bio11(最冷季度平均温)、bio5(最热月份最高温)、bio7(年温度变化范围)、bio8(最湿季度平均温);1个降水因子为bio15(雨量变化方差)。
在0.01水平上,与太子参皂苷含量呈显著负相关的综合气候因子为bio3(昼夜温差与年温差比值)、bio11(最冷季度平均温)、bio15(雨量变化方差),说明温度变化较大且降水量稳定的地区有利于太子参皂苷的积累,同时最冷季度时的低温有助于太子参皂苷的形成。与太子参皂苷含量呈显著正相关的综合气候因子为bio5(最热月份最高温)、bio7(年温度变化范围)、bio8(最湿季度平均温),说明最热季节温度越高越有利于太子参皂苷的积累。
2.2.3 月均因子
基于1-12月的月均因子,计算其与太子参皂苷含量的相关系数(图4,表3 ~ 表5)。
表 3 太子参皂苷含量与月均降水的Pearson系数Table 3. Pearson correlation coefficients between mean monthly precipitation and saponin content综合气候因子
Climate factor相关性
Correlation显著性(双尾)
Sig.综合气候因子
Climate factor相关性
Correlation显著性(双尾)
Sig.prec_1 0.339 0.235 prec_7 0.891** 0.000 prec_2 0.230 0.429 prec_8 −0.556* 0.039 prec_3 −0.044 0.880 prec_9 −0.461 0.097 prec_4 −0.576* 0.031 prec_10 −0.950** 0.000 prec_5 −0.906** 0.000 prec_11 −0.719** 0.004 prec_6 −0.630* 0.016 prec_12 0.315 0.272 注:* 表示 0.05 级别(双尾)相关性显著。下同。 Note: * indicates significant differences at P < 0.05 level. Same below. 表 5 太子参皂苷含量与月均水汽压的Pearson系数Table 5. Pearson correlation coefficients between mean monthly vapor pressure and saponin content综合气候因子
Climate factor相关性
Correlation显著性(双尾)
Sig.综合气候因子
Climate factor相关性
Correlation显著性(双尾)
Sig.vapr_1 −0.864** 0.000 vapr_7 0.944** 0.000 vapr_2 −0.850** 0.000 vapr_8 0.942** 0.000 vapr_3 −0.860** 0.000 vapr_9 0.744** 0.002 vapr_4 −0.811** 0.000 vapr_10 0.194 0.506 vapr_5 −0.316 0.271 vapr_11 −0.618* 0.019 vapr_6 0.673** 0.008 vapr_12 −0.886** 0.000 太子参皂苷含量与每月平均气温呈现出负相关-正相关-负相关的动态变化趋势,即与最冷季节的月均温(1-4月、11-12月)呈显著负相关,说明最冷季度的低温有助于太子参皂苷的积累。而与最热季节(5-9月)的月均温呈正相关,说明最热季节的月均温对太子参皂苷的积累有促进作用,这与2.2.2中的结论一致。另外,2.2.1中的分析结果显示太子参皂苷含量与年均温相关性不显著,为弱负相关,但月均气温的相关性结果显示太子参皂苷含量与月均气温呈现全年的动态变化趋势。因此,月均尺度上更能真实准确地反映化学成分含量与气候因子的动态响应关系,并能得出化学成分含量累积的主要时间段及时间窗口。
由表3可知,太子参皂苷含量与每月平均降水量呈现出弱正相关-强负相关-弱正相关的动态变化趋势,说明对太子参皂苷含量影响比较大的时间窗口是强负相关的4-11月,即除了7月平均降水量与太子参皂苷含量呈正相关,其余4-6月、8-11月均与太子参皂苷含量呈负相关,而1-2月和年底的12月却与太子参皂苷含量呈正相关。2.2.1和2.2.2中的分析结果分别表明太子参皂苷含量与年均降水量呈负相关,与雨量变化方差(bio15)呈负相关,说明均匀降水有助于太子参皂苷累积,同时也说明了月均因子比年均因子更能准确反映出气候因子对太子参皂苷含量的动态影响。
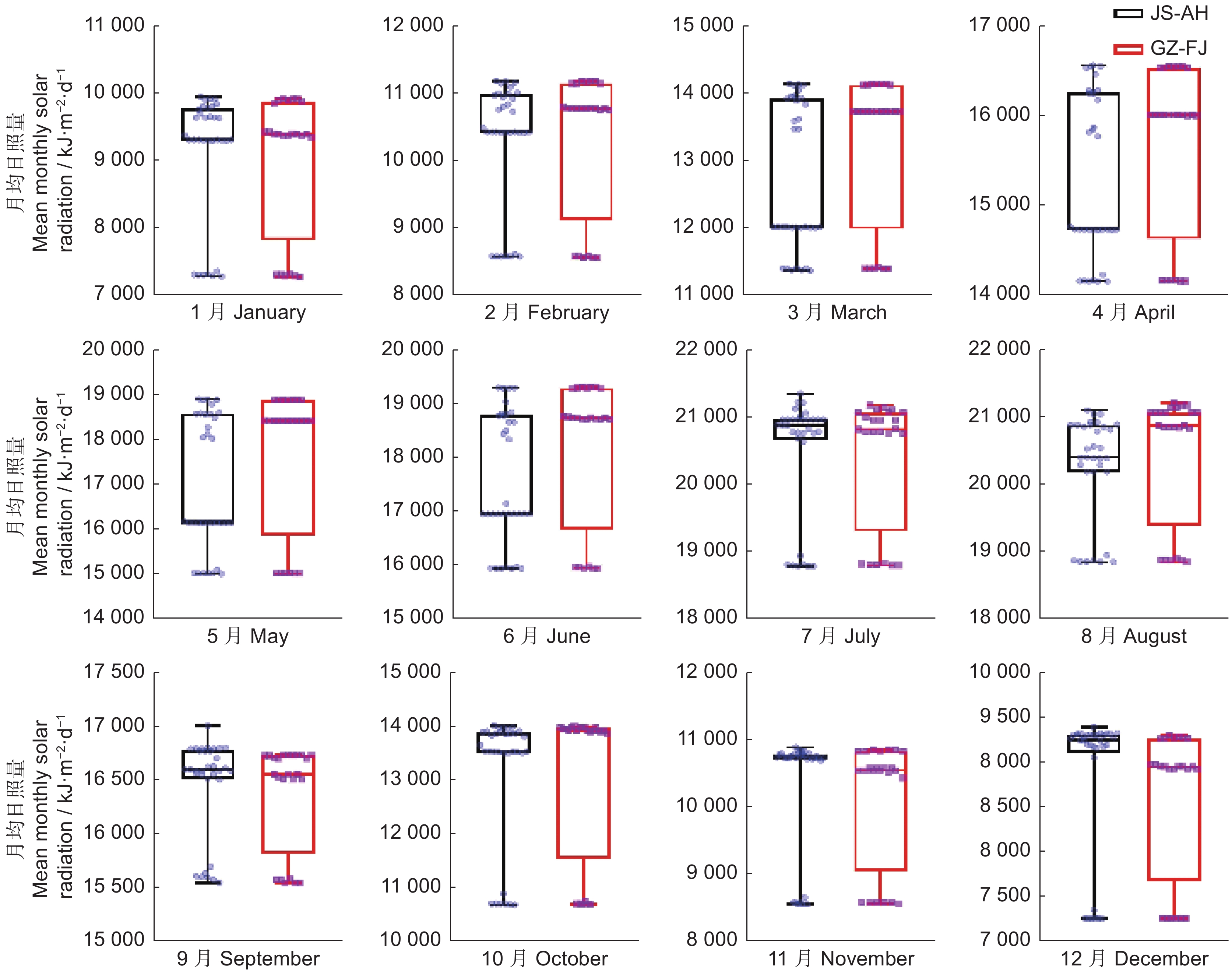
表4结果显示,在0.01水平上,1-12月的月均日照量均与太子参皂苷含量呈极显著正相关,说明月均日照量对太子参皂苷的合成和积累有着至关重要的影响,月均日照量越长,太子参皂苷积累也就越多,与2.2.1中与年均日照时数呈强正相关的结论相呼应。其中相关系数大于0.9的月份有3-6月,说明这几个月的月均日照量对太子参皂苷含量积累的影响最为关键。
表 4 太子参皂苷含量与月均日照量的Pearson系数Table 4. Pearson correlation coefficients between mean monthly solar radiation and saponin content综合气候因子
Climate factor相关性
Correlation显著性(双尾)
Sig.综合气候因子
Climate factor相关性
Correlation显著性(双尾)
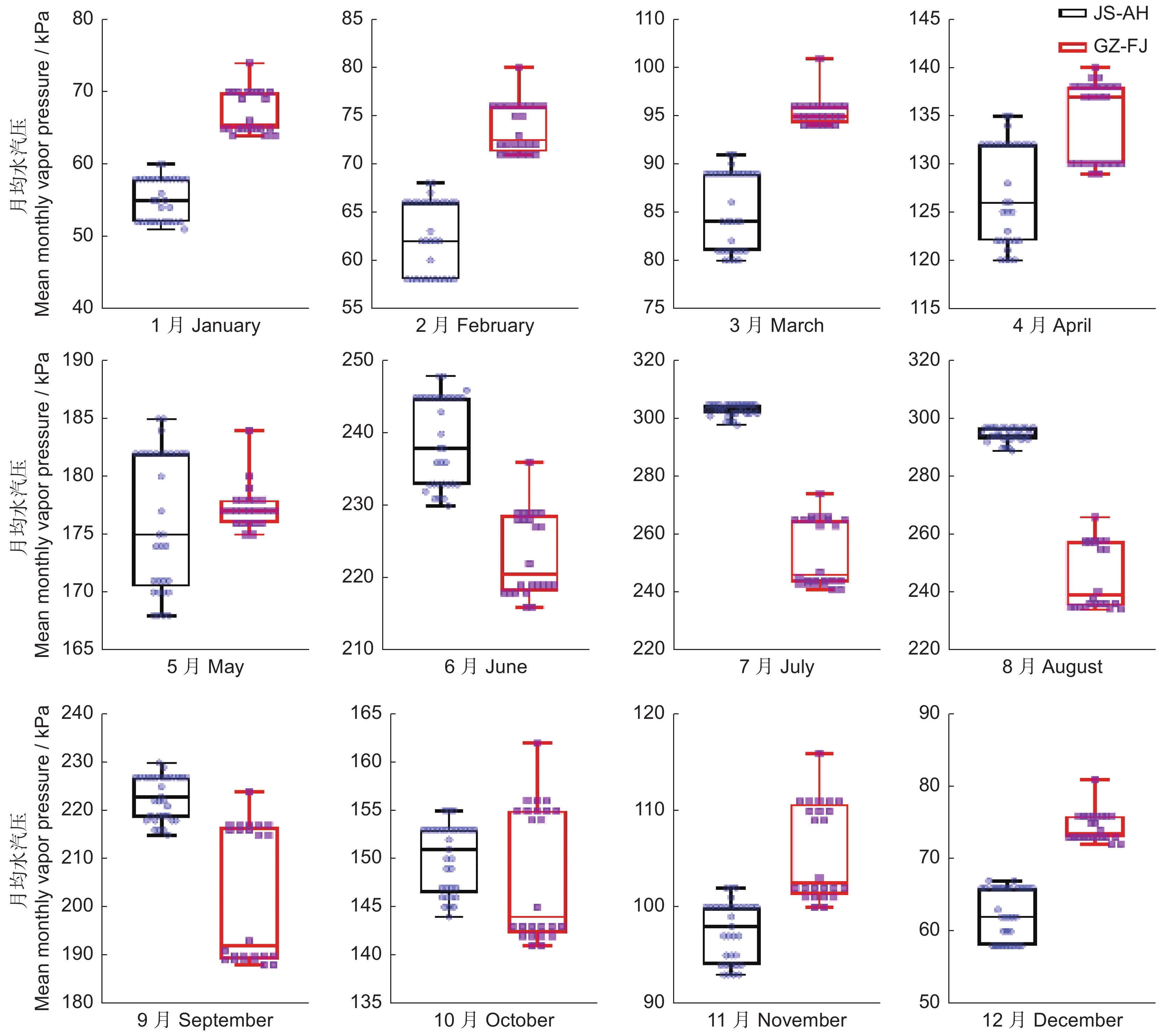
Sig.srad_1 0.872** 0.000 srad_7 0.668** 0.009 srad_2 0.889** 0.000 srad_8 0.827** 0.000 srad_3 0.990** 0.000 srad_9 0.596* 0.024 srad_4 0.984** 0.000 srad_10 0.838** 0.000 srad_5 0.986** 0.000 srad_11 0.785** 0.001 srad_6 0.975** 0.000 srad_12 0.770** 0.001 表5分析结果显示,太子参皂苷含量与月均水汽压呈负相关-正相关-负相关的动态变化,其中,1-4月以及11-12月的月均水汽压与太子参皂苷含量呈强负相关,说明在这期间较低的月均水汽压更适宜太子参皂苷的合成和积累。太子参皂苷含量与6-9月的月均水汽压呈极显著正相关,说明在此期间较高的月均水汽压有利于太子参皂苷的积累。
综上结果可见,太子参皂苷含量与月均日照量全年响应关系一致,为显著正相关,而与其他3个月均因子呈现不同的动态变化趋势,即与月均气温的响应关系为负相关-正相关-负相关,与每月平均降水量呈现出正相关-负相关-正相关的动态变化趋势,与月均水汽压呈现出负相关-正相关-负相关的趋势。
2.2.4 太子参皂苷不同含量区气候特征
江苏和安徽地区的太子参皂苷含量高,而贵州和福建地区含量低;太子参皂苷含量与月均温、月均日照量、月均降水量和月均水汽压均有强相关性。为说明江苏-安徽皂苷高含量区和贵州-福建低含量区的气候差异,本研究分析了上述3个月均因子在太子参不同品质区的动态差异情况(图5 ~ 图7)。
由图5可知,江苏-安徽地区的月均温在1-3月高于该地区,4-9月低于该地区,而10-12月又高于该地区。同时,月均平均气温与太子参皂苷含量呈负相关-正相关-负相关的动态变化趋势(图4)。因此,气温对于太子参皂苷含量的影响,江苏-安徽地区的太子参皂苷含量低于贵州-福建地区。
贵州-福建地区的月均日照量均高于江苏-安徽地区,而月均日照量与太子参皂苷含量呈正相关,因此若只考虑日照量对太子参皂苷含量的影响,贵州-福建地区的太子参皂苷含量要高于江苏-安徽地区(图6)。江苏-安徽地区的月均水汽压在1-5月份低于贵州-福建地区,6-10月份高于该地区,11-12月又低于该地区(图7)。表5分析结果说明月均水汽压与太子参皂苷含量的相关性呈负相关-正相关-负相关的动态趋势。因此,仅考虑月均水汽压对太子参皂苷含量的影响,江苏-安徽地区太子参皂苷累积要高于贵州-福建地区。
3. 讨论
3.1 太子参皂苷含量的地理变异
本研究发现,不同产地间的太子参皂苷含量存在明显的地理变异,可分为江苏-安徽太子参皂苷高含量型和贵州-福建太子参皂苷低含量型。其他学者也多次发现,不同地区太子参品质不同,如邹立思等[30]通过GC-MS分析发现江苏句容与福建柘荣两地栽培的太子参在挥发性成分上有明显区别。刘训红等[31]发现不同产地的太子参皂苷含量有一定差异。侯娅等[32]发现多个产地太子参间的化学成分差异显著。
太子参中化学成分很多,前期研究初步揭示太子参中的多糖与气候因子的关系不大,可能药材中某些化学成分是气候主导型成分,而有些成分是基因主导型成分。这或许是生态型物种和基因型物种的区别,需要对不同物种和不同成分进行大量深入研究。正是由于太子参品质存在地理变异才会有不同产区品质优劣之分和道地产区之说。
作者前期对人参(Panax ginseng C. A. Mey.)和西洋参(Panax quinquefolium L.)的研究表明[33, 34],人参皂苷都与年均温呈负相关,低温有助于皂苷积累。本文也发现太子参皂苷与温度呈负相关,是否皂苷是低温逆境胁迫的产物,同时,其他药材中的皂苷是否也有这个规律,这是课题组以后研究方向。
3.2 太子参皂苷含量与气候因子间的动态响应特征
太子参皂苷含量与年均气温、年均降水、年均日照量、年均相对湿度均有一定相关性。进一步研究发现,太子参皂苷含量与日照量呈全年强正相关,而与其他3个因子则呈现不同的动态变化趋势,即与每月平均气温呈负相关-正相关-负相关的趋势,与每月平均降水量呈弱正相关-强负相关-弱正相关的趋势,与月均水汽压呈负相关-正相关-负相关的变化趋势。
太子参皂苷含量显示与最热季节温度(最湿季度平均温bio8、最热月份最高温bio5)呈正相关,与最冷季节温度呈负相关(最冷季度平均温bio11);进一步研究表明其与每月平均气温呈负相关-正相关-负相关的动态变化趋势。由此可见,基于年-季-月这种不同时间尺度的气候因子研究体系,能更精准分析出化学成分含量与气候因子的动态响应特征。
本研究结果还表明,太子参皂苷含量与bio3(昼夜温差与年温差比值)呈显著负相关,说明气温变化不大的地区有利于皂苷积累。而康传志等[35]发现,最暖季平均温、等温性是影响太子参种植分布的最重要环境因子,与本研究结论一致。本研究还发现,在6-9月太子参的休眠期间,月均水汽压与太子参皂苷含量呈极显著正相关,其他研究[36, 37]也发现产地湿度较大,太子参长势较缓,不仅徒长状况明显,而且易腐烂或染病害。
3.3 太子参不同品质区气候特征
太子参皂苷含量受气候因子影响较大,可能是环境主导型化学成分。根据太子参生物学特性,太子参喜温暖湿润气候,忌高温强光,在10 ℃ ~ 20 ℃时生长旺盛,当气温超过 30 ℃时植株生长停滞。其耐寒性强,怕旱怕涝,产地湿度过高易造成渍水烂根以及腐烂感染[38, 39],这与本研究结果一致。在太子参不同品质区,如江苏-安徽高含量区和贵州-福建低含量区,4种气候因子的不同年度变化造就了太子参皂苷含量的差异,因此,在不同种植地区内采取适当的田间管理措施有助于改善药材品质,可为太子参的引种扩种和田间管理提供参考。
-
表 1 互作蛋白点对点验证所用引物
Table 1 Primers used in one-to-one verification of interacting proteins
引物名
Primer name正向序列(5′–3′)
Sequence of forward primer反向序列(5′–3′)
Sequence of reverse primerpGBKT7-NnWRKY40b CATGGAGGCCGAATTCATGGAGTC
GACTTGGTTGGATACGCAGGTCGACGGATCCTCACCA
TTTCTGCACTGTTGAATGpGADT7-NnJAZ1 CAGATTACGCTCATATGATGTCAA
GAGCGCCGGACCTTGCTTGGGTGGAATTCCTACTGT
GGAGATCGAGCTTGTpGADT7-NnUBC CAGATTACGCTCATATGATGGCGA
ACAGCAATCTACCCTGCTTGGGTGGAATTCTCAGGCA
CCACTTGCATATAGpGADT7-NnCHS CAGATTACGCTCATATGATGGTGA
CCGTGGAAGACATCTGCTTGGGTGGAATTCCTAGGCA
GCGATACTGTGAAGpGADT7-NnPEBP CAGATTACGCTCATATGATGGCGA
GTGACGAGTTTAGGTTGCTTGGGTGGAATTCTTAGGCT
GGGAAAAGTCGGATCpGADT7-NnPPOA CAGATTACGCTCATATGATGGCA
TCGCTTTCTCCCTTGATGCTTGGGTGGAATTCTCACGAA
GCGAACACTATCTTGpGADT7-Unknown protein3 CAGATTACGCTCATATGATGCAT
TCCCTGAGCTTAAAACTTGCTTGGGTGGAATTCTTAGACG
ATATCCGTATCATCTC表 2 NnWRKY40b互作蛋白筛选及其功能预测
Table 2 Screening and functional prediction of NnWRKY40b interacting proteins
分类
Classification蛋白号
Protein ID基因号
Gene ID蛋白名称
Protein name相关蛋白功能预测
Protein function prediction生长发育及
抗逆XP_010271938.1 LOC104607876 枯草杆菌蛋白酶,NnSBT1.7 种皮发育相关 XP_010266914.1 LOC104604316 质体蓝素,NnPC2B 参与光合作用 XP_010279114.1 LOC104613113 泛素结合酶,NnUBC DNA修复,光周期,抗逆胁迫响应,降解生长素,延缓植物衰老,调控ABA信号途径 YP_009093956.1 LOC20834983 ATP合成酶CF1亚基,NnatpE 光合作用,细胞代谢 XP_010265991.1 LOC104603626 类似谷胱甘肽S-转移酶U17, NnGST 抗逆反应,植物修复 XP_010269750.1 LOC104606314 铜转运蛋白5.1,NnCTR5.1 光合作用,呼吸作用,细胞壁代谢,氧化应激反应 XP_010255313.1 LOC104596029 非依赖性蛋白转位酶蛋白,NnTATB 细胞内运输、分泌和囊泡转运 XP_010248208.1 LOC104591115 二磷酸核酮糖羧化酶/加氧酶激活酶,NnRCA 光合作用,叶片衰老,响应非生物胁迫 XP_010270928.1 LOC104607108 半胱氨酸过氧化物氧还蛋白,NnPER1 细胞氧化还原稳态,细胞氧化剂解毒 XP_010269352.1 LOC104606034 60S核糖体蛋白L13e,NnRPL13 翻译、核糖体结构与生物发生 XP_010270872 LOC104607076 ADP-核糖基化因子,NnBLH8 细胞内运输、分泌和囊泡转运 XP_010275748.1 LOC104610704 核糖核酸酶,NnCAF 1 RNA降解 XP_010241640.1 LOC104586181 液泡蛋白分选相关蛋白,NnVPS37-1 盐胁迫响应 XP_010264580.1 LOC104602549 磷脂酰乙醇胺结合蛋白,NnPEBP 植物生长发育,几种信号通路的调节,如MAP激酶通路 XP_010251283.1 LOC104593218 类似Fcf2蛋白,NnFcf 胚成熟,花瓣分化,叶片衰老 XP_010263125.1 LOC104601478 ATP合成酶, NnatpH 光合作用,细胞代谢 XP_010244725.1 LOC104588480 类ACR12蛋白,NnACR12 光合电子传递,冷响应,光响应 激素调控和
次级代谢XP_010258950.1 LOC104598530 泛素蛋白,NnUBQ 蛋白降解,茉莉酸信号途径,细胞周期 XP_010251469.1 LOC104593386 类似TIFY 10A蛋白,NnJAZ1 抑制JA信号传导,响应盐胁迫,
花的发育,茎叶的发育NP_001305084.1 LOC104602160 查尔酮合成酶,NnCHS 类黄酮的生物合成,生长素运输的调节,根系向重力性的调节 XP_010273014.1 LOC104608661 DAHP合成酶,NnDAHP 分支酸合成 ADC92563.1 LOC104588895 多酚氧化酶,NnPPOA 类黄酮、木质素、原花青素生物合成过程 XP_010270953.1 LOC104607120 S-腺苷甲硫氨酸合酶5,NnSAMS 木质素生物合成过程,蛋氨酸代谢过程,冷反应 未知 XP_010261469.1 LOC104600297 未表征蛋白1 未知 XP_010260316.1 LOC104599465 未表征蛋白2 未知 XP_010248518.1 LOC104591415 未表征蛋白3 未知 XP_010276554.1 LOC104611264 未表征蛋白4 未知 -
[1] 陈强,张华,沙玫,刘永静. 一测多评法同时测定荷叶中4种生物碱含量[J]. 福建中医药,2020,51(6):29−32. doi: 10.3969/j.issn.1000-338X.2020.06.011 Chen Q,Zhang H,Sha M,Liu YJ. Simultaneous determination of four alkaloids in nelumbinis folium by quantitative analysis of multi-components by single marker[J]. Fujian Journal of Traditional Chinese Medicine,2020,51 (6):29−32. doi: 10.3969/j.issn.1000-338X.2020.06.011
[2] Wan Y,Xia J,Xu JF,Chen L,Yang Y,et al. Nuciferine,an active ingredient derived from lotus leaf,lights up the way for the potential treatment of obesity and obesity-related diseases[J]. Pharmacol Res,2022,175:106002. doi: 10.1016/j.phrs.2021.106002
[3] Abdallah BM,Ali EM. Green synthesis of silver nanoparticles using the Lotus lalambensis aqueous leaf extract and their anti-candidal activity against oral candidiasis[J]. ACS Omega,2021,6 (12):8151−8162. doi: 10.1021/acsomega.0c06009
[4] Tong YL,Li ZW,Wu YK,Zhu SL,Lu KK,He Z. Lotus leaf extract inhibits ER- breast cancer cell migration and metastasis[J]. Nutr Metab,2021,18 (1):20. doi: 10.1186/s12986-021-00549-0
[5] Van der Fits L,Memelink J. ORCA3,a jasmonate-responsive transcriptional regulator of plant primary and secondary metabolism[J]. Science,2000,289 (5477):295−297. doi: 10.1126/science.289.5477.295
[6] Kato N,Dubouzet E,Kokabu Y,Yoshida S,Taniguchi Y,et al. Identification of a WRKY protein as a transcriptional regulator of benzylisoquinoline alkaloid biosynthesis in Coptis japonica[J]. Plant Cell Physiol,2007,48 (1):8−18. doi: 10.1093/pcp/pcl041
[7] Suttipanta N,Pattanaik S,Kulshrestha M,Patra B,Singh SK,Yuan L. The transcription factor CrWRKY1 positively regulates the terpenoid indole alkaloid biosynthesis in Catharanthus roseus[J]. Plant Physiol,2011,157 (4):2081−2093. doi: 10.1104/pp.111.181834
[8] Agarwal P,Pathak S,Lakhwani D,Gupta P,Asif MH,Trivedi PK. Comparative analysis of transcription factor gene families from Papaver somniferum:identification of regulatory factors involved in benzylisoquinoline alkaloid biosynthesis[J]. Protoplasma,2016,253 (3):857−871. doi: 10.1007/s00709-015-0848-8
[9] Zhou ML,Memelink J. Jasmonate-responsive transcription factors regulating plant secondary metabolism[J]. Biotechnol Adv,2016,34 (4):441−449. doi: 10.1016/j.biotechadv.2016.02.004
[10] Tripathi S,Sangwan RS,Mishra B,Jadaun JS,Sangwan NS. Berry transcriptome:insights into a novel resource to understand development dependent secondary metabolism in Withania somnifera(Ashwagandha)[J]. Physiol Plant,2020,168 (1):148−173. doi: 10.1111/ppl.12943
[11] Hao XL,Xie CH,Ruan QY,Zhang XC,Wu C,et al. The transcription factor OpWRKY2 positively regulates the biosynthesis of the anticancer drug camptothecin in Ophiorrhiza pumila[J]. Hortic Res,2021,8 (1):7. doi: 10.1038/s41438-020-00437-3
[12] Eulgem T,Rushton PJ,Robatzek S,Somssich IE. The WRKY superfamily of plant transcription factors[J]. Trends Plant Sci,2000,5 (5):199−206. doi: 10.1016/S1360-1385(00)01600-9
[13] Ishiguro S,Nakamura K. Characterization of a cDNA encoding a novel DNA-binding protein,SPF1,that recognizes SP8 sequences in the 5′ upstream regions of genes coding for sporamin and β-amylase from sweet potato[J]. Mol Gen Genet,1994,244 (6):563−571. doi: 10.1007/BF00282746
[14] 向小华,吴新儒,晁江涛,杨明磊,杨帆,等. 普通烟草WRKY基因家族的鉴定及表达分析[J]. 遗传,2016,38(9):840−856. doi: 10.16288/j.yczz.16-016 Xiang XH,Wu XR,Chao JT,Yang ML,Yang F,et al. Genome-wide identification and expression analysis of the WRKY gene family in common tobacco (Nicotiana tabacum L. )[J]. Hereditas,2016,38 (9):840−856. doi: 10.16288/j.yczz.16-016
[15] Cormack RS,Eulgem T,Rushton PJ,Köchner P,Hahlbrock K,Somssich IE. Leucine zipper-containing WRKY proteins widen the spectrum of immediate early elicitor-induced WRKY transcription factors in parsley[J]. BBA-Gene Struct Expr,2002,1576 (1-2):92−100. doi: 10.1016/S0167-4781(02)00298-1
[16] 郑超,郑二松,王栩鸣,李冬月,杨勇,等. 水稻WRKY转录调控因子研究进展[J]. 生物技术通讯,2018,29(2):286−294. doi: 10.3969/j.issn.1009-0002.2018.02.026 Zheng C,Zheng ES,Wang XM,Li DY,Yang Y,et al. Research progress on rice WRKY transcription factors[J]. Letters in Biotechnology,2018,29 (2):286−294. doi: 10.3969/j.issn.1009-0002.2018.02.026
[17] 杨致荣,王兴春,薛金爱,孟令芝,李润植. 药用植物长春花WRKY转录因子的鉴定及表达谱分析[J]. 生物工程学报,2013,29(6):785−802. doi: 10.13345/j.cjb.2013.06.006 Yang ZR,Wang XC,Xue JA,Meng LZ,Li RZ. Identification and expression analysis of WRKY transcription factors in medicinal plant Catharanthus roseus[J]. Chinese Journal of Biotechnology,2013,29 (6):785−802. doi: 10.13345/j.cjb.2013.06.006
[18] Yamada Y,Nishida S,Shitan N,Sato F. Genome-wide profiling of WRKY genes involved in benzylisoquinoline alkaloid biosynthesis in California Poppy (Eschscholzia californica)[J]. Front Plant Sci,2021,2:699326.
[19] Wei HW,Chen SY,Niyitanga S,Liu T,Qi JM,Zhang LW. Genome-wide identification and expression analysis response to GA3 stresses of WRKY gene family in seed hemp (Cannabis sativa L. )[J]. Gene,2022,822:146290. doi: 10.1016/j.gene.2022.146290
[20] Mishra S,Triptahi V,Singh S,Phukan UJ,Gupta MM,et al. Wound induced tanscriptional regulation of benzylisoquinoline pathway and characterization of wound inducible PsWRKY transcription factor from Papaver somniferum[J]. PLoS One,2013,8 (1):e52784. doi: 10.1371/journal.pone.0052784
[21] He J,Bouwmeester HJ,Dicke M,Kappers IF. Transcriptional and metabolite analysis reveal a shift in direct and indirect defences in response to spider-mite infestation in cucumber (Cucumis sativus)[J]. Plant Mol Biol,2020,103 (4-5):489−505. doi: 10.1007/s11103-020-01005-y
[22] 代红洋,柏旭,李晓岗,张兴开,罗霖,等. 植物激素在三萜类化合物生物合成中的作用及调控机制研究进展[J]. 中草药,2021,52(20):6391−6402. Dai HY,Bai X,Li XG,Zhang XK,Luo L,et al. Research progress on roles of phytohormone in biosynthesis of triterpenoids and their regulatory mechanisms[J]. Chinese Traditional and Herbal Drugs,2021,52 (20):6391−6402.
[23] Wasternack C,Song SS. Jasmonates:biosynthesis,metabolism,and signaling by proteins activating and repressing transcription[J]. J Exp Bot,2017,68 (6):1303−1321.
[24] Yang J,Duan GH,Li CQ,Liu L,Han GY,et al. The crosstalks between jasmonic acid and other plant hormone signaling highlight the involvement of jasmonic acid as a core component in plant response to biotic and abiotic stresses[J]. Front Plant Sci,2019,10:1349. doi: 10.3389/fpls.2019.01349
[25] Ming R,VanBuren R,Liu YL,Yang M,Han YP,et al. Genome of the long-living sacred lotus (Nelumbo nucifera Gaertn. )[J]. Genome Biol,2013,14 (5):R41. doi: 10.1186/gb-2013-14-5-r41
[26] Zhang Y,Rahmani RS,Yang XY,Chen JM,Shi T. Integrative expression network analysis of microRNA and gene isoforms in sacred lotus[J]. BMC Genomics,2020,21 (1):429. doi: 10.1186/s12864-020-06853-y
[27] Li J,Xiong YC,Li Y,Ye SQ,Yin Q,et al. Comprehensive analysis and functional studies of WRKY transcription factors in Nelumbo nucifera[J]. Int J Mol Sci,2019,20 (20):5006. doi: 10.3390/ijms20205006
[28] Ferrer JL,Austin MB,Stewart C Jr,Noel JP. Structure and function of enzymes involved in the biosynthesis of phenylpropanoids[J]. Plant Physiol Biochem,2008,46 (3):356−370. doi: 10.1016/j.plaphy.2007.12.009
[29] Ren GH,Wang BJ,Zhu XD,Mu Q,Wang C,et al. Cloning,expression,and characterization of miR058 and its target PPO during the development of grapevine berry stone[J]. Gene,2014,548 (2):166−173. doi: 10.1016/j.gene.2014.07.021
[30] 王馨雨,杨绿竹,王婷,王蓉蓉,刘洁,等. 植物多酚氧化酶的生理功能、分离纯化及酶促褐变控制的研究进展[J]. 食品科学,2020,41(9):222−237. doi: 10.7506/spkx1002-6630-20190411-145 Wang XY,Yang LZ,Wang T,Wang RR,Liu J,et al. Recent progress toward understanding the physiological function,purification,and enzymatic browning control of plant polyphenol oxidases[J]. Food Science,2020,41 (9):222−237. doi: 10.7506/spkx1002-6630-20190411-145
[31] 田娇,刘园,房敏峰. 外源茉莉酸类激素对药用植物次生代谢的影响研究[J]. 天然产物研究与开发,2015,27(1):185−190. doi: 10.16333/j.1001-6880.2015.01.037 Tian J,Liu Y,Fang MF. Review on the influence of exogenous jasmonates on medicinal plant secondary metabolism[J]. Natural Product Research and Development,2015,27 (1):185−190. doi: 10.16333/j.1001-6880.2015.01.037
[32] 王金利,史胜青,贾利强,江泽平. 植物泛素结合酶E2功能研究进展[J]. 生物技术通报,2010(4):7−10. doi: 10.13560/j.cnki.biotech.bull.1985.2010.04.002 Wang JL,Shi SQ,Jia LQ,Jiang ZP. Progress on functions of ubiquitin-conjugating enzyme (E2) in plants[J]. Biotechnology Bulletin,2010 (4):7−10. doi: 10.13560/j.cnki.biotech.bull.1985.2010.04.002
[33] 李兴芬,苗雅慧,孙永江,张孟娟,张凌云. 青杄PwPEBP基因及其启动子序列的克隆与表达分析[J]. 北京林业大学学报,2019,41(4):8−20. Li XF,Miao YH,Sun YJ,Zhang MJ,Zhang LY. Cloning and expression analysis of PwPEBP gene and promoter sequence in Picea wilsonii[J]. Journal of Beijing Forestry University,2019,41 (4):8−20.
[34] 王寻,高凝,张富军,韩月彭,王小非,等. 苹果磷脂酰乙醇胺结合蛋白PEBP家族基因的鉴定与比较分析[J]. 植物生理学报,2021,57(10):1996−2010. doi: 10.13592/j.cnki.ppj.2020.0395 Wang X,Gao N,Zhang FJ,Han YP,Wang XF,et al. Identification and comparative analysis of phosphatidyl ethanolamine binding protein (PEBP) family gene in apple[J]. Plant Physiology Journal,2021,57 (10):1996−2010. doi: 10.13592/j.cnki.ppj.2020.0395
[35] 祝一文,车永梅,赵方贵,朱丹,刘新. 碱胁迫下H2S参与活性氧代谢和水稻幼苗生长的调控[J]. 农业生物技术学报,2018,26(7):1124−1131. Zhu YW,Che YM,Zhao FG,Zhu D,Liu X. H2S functions in growth regulation in rice (Oryza sativa) seedling and metabolism modulating of reactive oxygen under alkaline stress[J]. Journal of Agricultural Biotechnology,2018,26 (7):1124−1131.
[36] 张金梅,白雪,李玥莹,张颖. WRKY响应植物逆境的“角色”[J]. 安徽农业科学,2020,48(12):5−8. doi: 10.3969/j.issn.0517-6611.2020.12.002 Zhang JM,Bai X,Li YY,Zhang Y. WRKY’s “Role” in response to plant adversity[J]. Journal of Anhui Agricultural Sciences,2020,48 (12):5−8. doi: 10.3969/j.issn.0517-6611.2020.12.002
[37] 魏昕,刘雨恒,刘宇阳,殷晓浦,谢恬,等. 植物JAZ蛋白家族研究进展[J]. 植物生理学报,2021,57(5):1039−1046. doi: 10.13592/j.cnki.ppj.2020.0532 Wei X,Liu YH,Liu YY,Yin XP,Xie T,et al. Advances of JAZ family in plants[J]. Plant Physiology Journal,2021,57 (5):1039−1046. doi: 10.13592/j.cnki.ppj.2020.0532
[38] Chini A,Fonseca S,Fernández G,Adie B,Chico JM,et al. The JAZ family of repressors is the missing link in jasmonate signalling[J]. Nature,2007,448 (7154):666−671. doi: 10.1038/nature06006
[39] Thines B,Katsir L,Melotto M,Niu YJ,Mandaokar A,et al. JAZ repressor proteins are targets of the SCFCOI1 complex during jasmonate signalling[J]. Nature,2007,448 (7154):661−665. doi: 10.1038/nature05960
[40] Chen XZ,Li JR,Liu YT,Wu DD,Huang HL,et al. PatSWC4,a methyl jasmonate-responsive MYB (v-myb avian myeloblastosis viral oncogene homolog)-related transcription factor,positively regulates patchoulol biosynthesis in Pogostemon cablin[J]. Ind Crops Prod,2020,154:112672. doi: 10.1016/j.indcrop.2020.112672
-
期刊类型引用(1)
1. 裴莉昕,陈琳,王锴乐,纪宝玉. 基于“气候因子-成分含量-抗氧化能力”评价不同产地葛根品质关系. 中国实验方剂学杂志. 2024(10): 140-148 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: